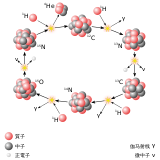
同中子素
外观
(重定向自同中子異荷素)

同中子素(英語:Isotone),又稱同中子異荷素、同中子異位核種[1],是指中子數相同而質子數不同的核種。例如:15
7N
與16
8O
都具有8個中子,故互為同中子素。由於質子數(原子序)不同,同中子素必然是不同的元素。
同中子素的英文isotone是將英文同位素(英語:Isotope)中的「p」替換成代表中子的「n(neutron)」而來。[2]該詞由德國物理學家K.古根海瑪(K. Guggenheimer)所創。[3]
穩定性
[编辑]中子數為偶數(尤其是2、8、20、28、50、82及126等幻數)的同中子素通常具有較高的穩定性,所含的穩定核種較多。82是具有最多穩定同中子素的中子數目,有6種穩定核種都具有82個中子。20和50其次,各有5種穩定的同中子素。
- 中子數為20的穩定核種:36
16S
、37
17Cl
、38
18Ar
、39
19K
、40
20Ca - 中子數為50的穩定核種:86
36Kr
、88
38Sr
、89
39Y
、90
40Zr
、92
42Mo - 中子數為82的穩定核種:138
56Ba
、139
57La
、140
58Ce
、141
59Pr
、142
60Nd
、144
62Sm
中子數為奇數的同中子素中所含的穩定核種數量大多不超過1種,除了1(2
1H
及3
2He
)、5(9
4Be
及10
5B
)、7(13
6C
及14
7N
)、55(97
42Mo
及99
44Ru
)和107(179
72Hf
及180m
73Ta
)。
沒有穩定核種的中子數目包括19、21、35、39、45、61、89、115、123和127以上的數目。至於沒有穩定核種的質子數目為43(鎝)、61(鉕)和83(鉍)以上的數目。
参閱
[编辑]參考資料
[编辑]- ^ 葉錫溶 蔡長書. 放射化學(第二版). 台灣台北縣: 新文京開發出版股份有限公司. 2008-03-26. ISBN 978-986-150-830-6 (中文(臺灣)).
- ^ Pauling, Linus. General Chemistry
 . Dover. 1998: 94. ISBN 0-486-65622-5.
. Dover. 1998: 94. ISBN 0-486-65622-5.
- ^ Nuclear Medicine Begins with a Boa Constrictor (页面存档备份,存于互联网档案馆), By Marshall Brucer, J Nucl Med 19: 581-598, 1978