硫化钠
外观
(重定向自硫化鈉)
| 硫化钠 | |
|---|---|

| |
| |
| 别名 | Sodium sulfide |
| 识别 | |
| CAS号 | 1313-82-2 1313-84-4(九水) |
| PubChem | 237873 |
| ChemSpider | 14120 |
| SMILES |
|
| InChI |
|
| InChIKey | GRVFOGOEDUUMBP-UHFFFAOYAP |
| UN编号 | 1385(无水) 1849(水合物) |
| EINECS | 215-211-5 |
| ChEBI | 76208 |
| RTECS | WE1905000 |
| 性质 | |
| 化学式 | 无水:Na2S 九水:Na2S · 9H2O |
| 摩尔质量 | 无水:78.046 g/mol 九水:240.182 g·mol⁻¹ |
| 外观 | 无色潮解固体 |
| 熔点 | 1180 °C (无水) |
| 溶解性(水) | 可溶 |
| 相关物质 | |
| 其他阴离子 | 氧化钠、硒化钠、碲化钠、钋化钠 |
| 其他阳离子 | 硫化鋰、硫化鉀、硫化銣、硫化銫 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
硫化钠是一种无机盐,化学式为Na2S,通常以九水合物Na2S·9H2O的形式存在。无水物和九水合物都是无色可溶的固体,在水溶液中水解呈强碱性。露置在空气中时,硫化钠会放出有臭鸡蛋气味的剧毒硫化氢气体。
性质
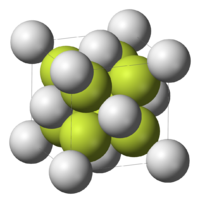
[编辑]Na2S有反萤石结构,Na+取代了CaF2中F−的位置,S2−则取代了Ca2+的位置。在溶液中S2−会强烈水解,分别生成HS−和H2S,而使溶液呈强碱性:
- S2− + H2O → HS− + OH−
- HS− + H2O ⇌ H2S + OH−
硫化钠能溶解硫生成多硫化钠(Na2Sx)。
生产
[编辑]工业上由焦炭(高温转炉、1373K)还原Na2SO4来制备Na2S。[1]
- Na2SO4 + 4C → Na2S + 4CO
也可通过氢气(沸腾炉、1373K)还原Na2SO4来制备Na2S。
- Na2SO4 + 4H2 → Na2S + 4H2O
实验室中可由钠和硫在氨中或萘的存在下于四氢呋喃中反应来制备无水硫化钠。[2]
- 2Na + S → Na2S
- H2S + 2NaOH → Na2S + 2H2O
安全
[编辑]Na2S及其水合物有毒,使用时需注意。其水溶液呈强碱性,会腐蚀皮肤,且会与酸迅速反应放出剧毒硫化氢气体。 离子方程式: S2- +2H+ =H2S↑
参见
[编辑]参考资料
[编辑]- ^ Holleman, A. F.; Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001. ISBN 0-12-352651-5.
- ^ J.-H. So and P. Boudjouk. N. G. Russell , 编. Hexamethyldisilathiane. Inorganic Syntheses. 1992. doi:10.1002/9780470132609.ch11.
