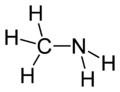
甲胺
| 甲胺 | |||
|---|---|---|---|
| |||

| |||
| IUPAC名 aminomethane 氨基甲烷 | |||
| 别名 | MMA | ||
| 识别 | |||
| CAS号 | 74-89-5 | ||
| SMILES |
| ||
| RTECS | PF6300000 | ||
| 性质 | |||
| 化学式 | CH5N | ||
| 摩尔质量 | 31.06 g·mol−1 | ||
| 密度 | d40.699 (−10.8 °C) / 0.902 g/cm³, 40w/w% (水) | ||
| 熔点 | −94 °C (179.15 K) | ||
| 沸点 | −6 °C (267.2 K) | ||
| 溶解性(水) | 108 g/100 mL (20 °C) | ||
| pKa | 10.64 (质子胺, pKaH) | ||
| pKb | 3.36 | ||
| 黏度 | 0.23 cP at 0 °C | ||
| 结构 | |||
| 分子构型 | 四面体 | ||
| 偶极矩 | 1.31 D (气体) | ||
| 危险性 | |||
| 警示术语 | R:R11-R36/37 (40%水溶液) | ||
| MSDS | EMD Chemicals [1] | ||
| 主要危害 | 有毒液体和气体,吸入危险,易燃 | ||
| NFPA 704 | |||
| 闪点 | 8 °C | ||
| 相关物质 | |||
| 相关胺 | 氨 二甲胺 三甲胺 | ||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
甲胺是一种有机化合物,化学式CH3NH2,它是氨中的一个氢被甲基取代后所形成的衍生物。甲胺是最简单的伯胺。市售品一般是其甲醇、乙醇、四氢呋喃或水溶液,或作为无水气体在金属槽中加压储存。工业品常将无水气体加压后通过拖车运输。它有刺激的腥味。甲胺被用作合成很多其他化合物的原料,每年大约能生产上亿公斤。
生产
[编辑]工业上常用氨气和甲醇在硅铝酸盐催化下反应来制取甲胺,这个反应的副产物有二甲胺和三甲胺。反应动力学和反应物的配比决定三个产品的多少。[1]
- CH3OH + NH3 → CH3NH2 + H2O
每年有大约400百万千克甲胺通过这种方法被生产。
实验室中,甲胺的盐酸盐很容易通过盐酸和六亚甲基四胺或甲醛和氯化铵反应得到。[2]
- NH4Cl + H2CO → CH2=NH·HCl + H2O
- CH2=NH·HCl + H2CO + H2O → CH3NH2·HCl + HCOOH
无色的盐酸盐可以通过加入强碱反应得到甲胺。
化学家夏爾-阿道夫·武爾茨通过水解异氰酸甲酯和其相关化合物第一次制得甲胺。[3]
活性及应用
[编辑]甲胺是一个很好的亲核试剂,因为它几乎没有空间位阻。它在有机化学中的应用十分广泛。一些和其它简单试剂发生的反应有:与光气反应制取异氰酸甲酯,与二硫化碳和氢氧化钠反应制取甲基二硫代氨基甲酸钠,和碱性条件的氯仿反应制取异腈,和环氧乙烷反应制取N-甲基乙醇胺等。
通过甲胺生产的有代表性的化合物包括了药品麻黄素和茶碱,农药克百威、西维因和威百亩和溶剂N-甲基甲酰胺和N-甲基吡咯烷酮。一些表面活性剂的制取也需要甲胺参与反应。[3]
液态甲胺可以用作类似液氨的溶剂。它和液氨在某些方面有相似之处,但能更好地溶解有机物(类似地,作为溶剂,甲醇优于水)。[4]
生物化学
[编辑]在自然界,甲胺通常由腐败产生。[5]在植物叶绿体的管腔中,甲胺作为缓冲剂存在,能有效地清除阻碍ATP合成的质子。
安全
[编辑]甲胺的LD50(鼠)是2400 mg/m3。甲胺也是美国缉毒署(DEA)列在第一类的化合物(作为生产毒品甲基苯丙胺的前体)。
应急处理
[编辑]皮肤接触:立即脱去被污染的衣着,用大量流动清水冲洗,至少15min。就医。 眼睛接触:立即提起眼睑,用大量流动清水或生理盐水彻底冲洗至少15min。就医。 吸入:迅速脱离现场至空气新鲜处。保持呼吸道通畅。如呼吸困难,给予输氧。如呼吸停止,立即进行人工呼吸。就医。 食入:误服者用水漱口,给饮牛奶或蛋清。就医。 呼吸系统防护:空气中浓度超标时,建议佩戴自吸过滤式防毒面具(全面罩)。紧急事态抢救或撤离时,建议佩戴氧气呼吸器或空气呼吸器。 眼睛防护:呼吸系统防护中已作防护。 身体防护:穿防静电工作服。 手防护:戴橡胶手套。 其他:工作现场严禁吸烟、进食和饮水。工作毕,淋浴更衣。 泄漏应急处理:有害燃烧产物:一氧化碳、二氧化碳、氧化氮。 灭火方法:切断气源。若不能切断气源,则不允许熄灭泄漏处的火焰。喷水冷却容器,可能的话将容器从火场移至空旷处。灭火剂:雾状水、抗溶性泡沫、干粉、二氧化碳。[6]
參見條目
[编辑]参考文献
[编辑]- ^ Corbin D.R.; Schwarz S.; Sonnichsen G.C. Methylamines synthesis: A review. Catalysis Today. 1997, 37 (2): 71–102. doi:10.1016/S0920-5861(97)00003-5.
- ^ Marvel, C. S.; Jenkins, R. L. (1941). "Methylamine Hydrochloride". Org. Synth.; Coll. Vol. 1: 347.
- ^ 3.0 3.1 Karsten Eller, Erhard Henkes, Roland Rossbacher, Hartmut Höke "Amines, Aliphatic" in Ullmann's Encyclopedia of Industrial Chemistry, Wiley-VCH, Weinheim, 2005.
- ^ H. D. Gibbs. Liquid methylamine as a solvent, and a study of its chemical reactivity. J. Am. Chem. Soc. 1906, 28: 1395–1422. doi:10.1021/ja01976a009.
- ^ Thauer, R. K., "Biochemistry of Methanogenesis: a Tribute to Marjory Stephenson", Microbiology, 1998, 144, 2377-2406.
- ^ 一甲胺_济南金贵林化工有限公司