外切體複合物

外切体复合物(英語:exosome complex,或PM/Scl complex,上下文意思清楚时,可以直接称為exosome),简称外切酶体、外切体,是一种蛋白质复合物,能够降解各种不同的核糖核酸(RNA)。由于复合物表现为核糖核酸外切酶活性,所以被命名为外切体。外切体复合物只存在于真核细胞和古菌中;而细菌中则对应有组成和结构更为简单的“降解体”复合物来发挥类似的功能。
外切体的核心是一个由六个亚基组成的环状结构,外围的亚基都结合在这一环状结构上。在真核细胞中,这一核心存在于细胞质和细胞核(特别是核仁)等细胞区室中;在不同的区室中,与之结合的蛋白质也不尽相同,从而可以调控外切体的活性以特异性地降解特定区室的RNA底物。外切体的底物包括信使RNA(mRNA)、核糖体RNA(rRNA)以及多种非编码RNA。外切体具有核糖核酸外切酶功能,也就意味着它可以从RNA的一端(3'端)开始降解作用,而不是从特定位点开始剪切RNA。
虽然没有已知疾病与外切体直接相关,但复合物中的多个蛋白亚基是一些特定自體免疫性疾病(特别是“硬化性肌炎”(Scleromyositis))病人自身抗体的靶标,也是治疗癌症的一些抗代谢化学疗法(能够阻断外切体的活性)的靶标。
发现
[编辑]第一个外切体的发现是来自于对模式生物酿酒酵母的研究:1997年外切体首次在酿酒酵母中被发现,并被鉴定为一种核糖核酸酶。[1]两年之后,研究者发现外切体也存在于人体细胞中,实际上就是多年前发现的存在于特定自體免疫性疾病病人体内的一种被称为“PM/Scl复合物”的自身抗原,具体见#疾病一节。[2]对“PM/Scl复合物”的纯化使得越来越多的人源外切体亚基蛋白被发现,直到最后所有形成这一复合物的组分都得到鉴定。[3][4]2001年,日益增长的基因组数据使得对古菌中外切体蛋白的预测成为可能;[5]但直到2003年,来自古菌的外切体复合物才首次被纯化出来,从而确定了外切体在古菌中的存在。[6]
结构
[编辑]核心蛋白
[编辑]
外切体复合物的核心是一个由六个蛋白亚基所组成的一个环状结构,这六个蛋白质都属于同一类核糖核酸酶(核糖核酸酶PH类似蛋白,含有PH结构域)。[7]在古菌中,这六个蛋白亚基实际上为两种不同的PH类似蛋白(分别为Rrp41和Rrp42)重复出现三次而来。真核生物中的外切体的核心环结构则由六种不同的蛋白质构成;[8][9]在这六个蛋白质中,其中三个与古菌的Rrp41蛋白相似,另外三个则与 Rrp42蛋白相似。[10]
结合在核心环状结构顶部的三个蛋白质都含有S1结构域(一种RNA结合结构域),其中两个蛋白质还含有KH结构域(K-homology domain,同样可以结合RNA)。[7]在真核生物中,含S1结构域的三个蛋白质都各不相同;而在古菌中,这三个蛋白质是相同的或至少其中有两个是相同的。[11]

相似的环状结构也存在于核糖核酸酶PH和多核苷酸磷酸化酶(PNPase)中。细菌中的核糖核酸酶PH,参与tRNA的处理,同样可以形成一个由六个相同的核糖核酸酶PH蛋白组成的六元环复合物。[12][13]以多核苷酸磷酸化酶为例,它是一种能够降解磷酸化的RNA的蛋白质,存在于细菌和一些真核生物的叶绿体和线粒体中,它的结构中既含有两个PH结构域又含有一个S1结构域和一个KH结构域;多核苷酸磷酸化酶可以形成同源三聚体复合物,其构象与外切体的环状结构非常相似。[14]因为在结构域组成和结构上的相似性,外切体和这两个复合物被认为在进化上有联系,可能具有共同祖先。[15]外切体的核糖核酸酶PH类似蛋白、核糖核酸酶PH以及多核苷酸磷酸化酶都属于核糖核酸酶PH蛋白家族,为磷酸解核酸外切酶(使用磷酸盐作为亲核攻击分子来从RNA分子的3'端去除核苷酸)。[7]
外围蛋白
[编辑]除了九个核心蛋白之外,真核生物的外切体中还往往包含两个能够与核心结合的蛋白质。其中之一是Rrp44蛋白,一种水解核糖核酸酶,属于核糖核酸酶R水解核酸外切酶(利用水分子来剪切核苷键)蛋白家族。在酵母中,Rrp44可以和“所有”的外切体复合物结合,并且对于酵母外切体的活性的发挥起着关键作用。[16]值得一提的是,虽然人体中也存在Rrp44的同源蛋白,但目前没有证据显示这一同源蛋白可以与人源外切体复合物结合。[7]

第二个常见的结合蛋白质是Rrp6(酵母中)或PM/Scl-100(人体中)。与Rrp44相似,这一蛋白质也是水解核糖核酸外切酶,但它属于核糖核酸酶D蛋白家族。[17]PM/Scl-100蛋白在细胞核中的外切体复合物中最为常见,但也可以参与形成细胞质中的外切体复合物。[18]
调节蛋白
[编辑]在这两个能够与核心紧密结合的亚基之外,还有许多蛋白质可以与外切体复合物在细胞核内或核外相互作用。这些较松散结合的蛋白质可能可以调控外切体的活性和特异性。在细胞质中,外切体可以与AU富含元素(AU rich element)结合蛋白(如KRSP和TTP,它们可以促进或阻碍mRNA的降解)相互作用;而细胞核中的外切体可以与控制核糖体RNA处理的RNA结合蛋白(如人体中的MPP6以及人和酵母中的Rrp47/C1D)相互结合。[7]
除了单个蛋白质以外,还有一些蛋白质复合物可以与外切体相互作用。其中之一便是细胞质中的Ski复合物,Ski复合物中包含了一个RNA螺旋酶(Ski2)并参与了RNA的降解。[19]在细胞核中,外切体对rRNA和小核仁RNA的降解是在TRAMP复合物(同时具有RNA螺旋酶和多聚腺苷酸化活性)的介导下进行的。[20]
功能
[编辑]催化作用
[编辑]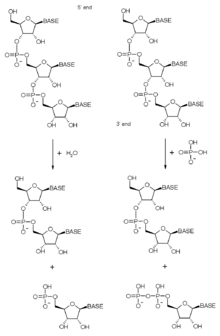
如前所述,外切体复合物中的多个蛋白亚基都含有核糖核酸酶结构域。这些结构域都属于3'-5'的核糖核酸外切酶结构域,也就是说含有这些结构域的蛋白质(酶)是从RNA分子的3'端开始对其进行降解。外切体中含有磷酸解的外切酶(核糖核酸酶PH类似蛋白),在真核生物中还含有水解型外切酶(核糖核酸酶R和核糖核酸酶D结构域蛋白)。磷酸解型酶利用无机磷酸根来剪切磷酸双酯键,并生成二磷酸核苷酸;而水解型酶则利用水分子来水解磷酸双酯键,并释放单磷酸核苷酸。
在古菌中,外切体复合物中的Rrp41亚基属于磷酸解的外切酶。核心环中的三个Rrp41亚基负责发挥复合物的酶解活性。[9]在真核生物中,外切体中的核糖核酸酶PH亚基都没有保留催化活性,因此其所组成的核心环没有酶活性。[21]在酵母中,外切体的核糖核酸酶活性主要是由外周蛋白亚基Rrp44(水解型外切酶)来发挥,[22]但这一特定亚基只被发现存在于酵母,目前并没有在人或古菌的外切体复合物中找到其同源蛋白。[21][23]此外,在人和酵母中都存在另一个可以与外切体结合的水解型外切酶(Rrp6),它是人源外切体中的活性来源,对酵母外切体的活性也有贡献。含S1结构域的蛋白亚基原本被认为也具有外切酶活性,但最近的研究结果对这一看法提出质疑,并认为其作用可能只是结合底物以利于外切体对底物的降解。[22]

底物
[编辑]
外切体参与降解和处理大量各种不同的RNA底物。在细胞质中,它参与mRNA分子的更新:外切体复合物可以通过与无义介导的降解或无终止降解通路中的蛋白质相互作用来降解被标记需要进行降解的mRNA分子(包含了错误信息的mRNA)。另外,mRNA的正常更新过程也需要外切体参与的降解过程。多个蛋白质可以通过结合到与外切体复合物结合的mRNA的3'端AU富含元素上来使mRNA稳定或不稳定。[24][25][26]在细胞核中,外切体对于多种小核RNA分子的正确处理是必不可少的。[27]核仁是外切体复合物的主要聚集区域。在核仁中,外切体参与了对5.8S核糖体RNA(外切体的第一个被发现的功能)和数种小核RNA的处理。[1][27][28]
虽然大多数的细胞都含有其他可以降解RNA的酶,可以从无论是3'还是5'端对RNA进行降解,但外切体复合物对细胞的存活依然必不可少。如果外切体中的蛋白质的表达被人为(例如通过RNA干扰)降低或停止,细胞就会停止生长并逐渐死亡。外切体复合物的核心蛋白以及两个主要的结合蛋白是细胞中的必要蛋白质。[29]细菌中不含有外切体复合物,相似的功能是由一个更简单的复合物──降解体来执行。[30]
疾病
[编辑]自體免疫
[编辑]外切体复合物是获患自體免疫性疾病病人的自身抗体的靶标。这些自身抗体被发现主要存在于患有PM/Scl重叠综合征(一种自體免疫性疾病,同时具有硬皮病和多发性肌炎病征)的病人体内。[31]自身抗体可以用病人的血清通过多种检验方法获得检测。过去最为常用的检测方法是采用双向免疫扩散法(使用小牛胸腺提取物)、免疫荧光(对HEp-2细胞)或免疫共沉淀(来自人体细胞的提取物)。在免疫共沉淀分析中,用抗外切体为阳性的血清,可以沉淀出一系列不同的蛋白质(即外切体复合物中的各个蛋白亚基),在外切体复合物被发现之前,它们被称为“PM/Scl复合物”。[32]用来自病人的血清进行免疫荧光分析,可以看到细胞的核仁被特定染色,表明被自身抗体所是别的抗原可能在核糖体的合成中发挥重要作用。[33]最近,重组的外切体蛋白已经可以被合成并用于在线免疫分析法(line immunoassay)和酶联免疫吸附法(ELISA)中来检测这些自身抗体。[7]
在这些疾病中,抗体主要是直接识别外切体复合物中的两个蛋白亚基,PM/Scl-100(核糖核酸酶D类似蛋白)和PM/Scl-75(核心环中核糖核酸酶PH类似蛋白之一),识别这两个蛋白质的抗体被发现存在于近30%患有PM/Scl重叠综合征的患者体内。[34]除了这两个主要的自身抗体的靶蛋白外,其他的外切体亚基和结合蛋白(如C1D)也可以被病人体内的自身抗体识别。[35][36]检测这些抗体最灵敏的方法是在ELISA中用一段来自PM/Scl-100蛋白上的肽段来代替整个PM/Scl-100蛋白作为抗原。采用这一方法已经在高达55%的PM/Scl重叠综合征病人体内发现相应的自身抗体,但这些抗体在其他只患有硬皮病、多发性肌炎或皮肌炎的病人体内也能被检测到。[37]
由于这些自身抗体主要发现于具有多种不同的自體免疫疾病病征的病人体内,这些病人的临床症状可能会具有很大差异。最常见的症状往往是单个自體免疫疾病所具有的典型症状,如雷诺氏综合征、关节炎、肌炎和硬皮症。[38]对这些病人的治疗与对单个自體免疫疾病的治疗相似,常常使用包括免疫抑制和免疫调控药物。[39]
癌症
[编辑]目前已发现外切体的活性可以被抗代谢物类药物氟尿嘧啶(fluorouracil)所抑制,而氟尿嘧啶是治疗癌症的化学疗法中使用的一种药物,并且是实体肿瘤治疗中最为成功的药物之一。在用氟尿嘧啶处理过的酵母细胞中,核糖体RNA的加工出现缺陷,这与外切体被分子生物学方法抑制后所观察到的现象一致。核糖体RNA无法正确被加工对于细胞而言是致命的,这也就解释了为什么氟尿嘧啶这类药物的抗代谢影响可以被用于杀死癌细胞。[40]
亚基列表
[编辑]| 图例 | 通用名 | 结构域 | 人源 | 酵母(S. cerevisiae) | 古菌 | 分子量(kD) | 人源基因 | 酵母基因 |
|---|---|---|---|---|---|---|---|---|
| 1 | Csl4 | S1 RBD | hCsl4 | Csl4p/Ski4p | Csl4 | 21-32 | EXOSC1 | YNL232W |
| 2 | Rrp4 | S1/KH RBD | hRrp4 | Rrp4p | Rrp4 | 28-39 | EXOSC2 | YHR069C |
| 3 | Rrp40 | S1/KH RBD | hRrp40 | Rrp40p | (Rrp4)[註 1] | 27-32 | EXOSC3 | YOL142W |
| 4 | Rrp41 | RNase PH | hRrp41 | Rrp41p/Ski6p | Rrp41 | 26-28 | EXOSC4 | YGR195W |
| 5 | Rrp46 | RNase PH | hRrp46 | Rrp46p | (Rrp41)[註 1] | 25-28 | EXOSC5 | YGR095C |
| 6 | Mtr3 | RNase PH | hMtr3 | Mtr3p | (Rrp41)[註 1] | 24-37 | EXOSC6 | YGR158C |
| 7 | Rrp42 | RNase PH | hRrp42 | Rrp42p | Rrp42 | 29-32 | EXOSC7 | YDL111C |
| 8 | Rrp43 | RNase PH | OIP2 | Rrp43p | (Rrp42)[註 1] | 30-44 | EXOSC8 | YCR035C |
| 9 | Rrp45 | RNase PH | PM/Scl-75 | Rrp45p | (Rrp42)[註 1] | 34-49 | EXOSC9 | YDR280W |
| 10 | Rrp6 | RNase D | PM/Scl-100 | Rrp6p | n/a | 84-100 | EXOSC10 | YOR001W |
| 11 | Rrp44 | RNase R | (hDis3)[註 2] | Rrp44p/Dis3p | n/a | 105-113 | KIAA1008 | YOL021C |
参见
[编辑]注释
[编辑]参考文献
[编辑]- ^ 1.0 1.1 Mitchell, Philip; Petfalski, Elisabeth; Shevchenko, Andrej; Mann, Matthias; Tollervey, David. The Exosome: A Conserved Eukaryotic RNA Processing Complex Containing Multiple 3′→5′ Exoribonucleases. Cell. 1997-11-14, 91 (4). ISSN 0092-8674. PMID 9390555. doi:10.1016/S0092-8674(00)80432-8 (英语).
- ^ Allmang, Christine; Petfalski, Elisabeth; Podtelejnikov, Alexandre; Mann, Matthias; Tollervey, David; Mitchell, Philip. The yeast exosome and human PM–Scl are related complexes of 3′ → 5′ exonucleases. Genes & Development. 1999-08-15, 13 (16) [2022-08-02]. ISSN 0890-9369. PMC 316947
 . PMID 10465791. doi:10.1101/gad.13.16.2148. (原始内容存档于2022-06-17) (英语).
. PMID 10465791. doi:10.1101/gad.13.16.2148. (原始内容存档于2022-06-17) (英语).
- ^ Brouwer, Rick; Allmang, Christine; Raijmakers, Reinout; Aarssen, Yvonne van; Egberts, Wilma Vree; Petfalski, Elisabeth; Venrooij, Walther J. van; Tollervey, David; Pruijn, Ger J. M. Three Novel Components of the Human Exosome *. Journal of Biological Chemistry. 2001-03-02, 276 (9). ISSN 0021-9258. PMID 11110791. doi:10.1074/jbc.M007603200 (英语).
- ^ Chen, Ching-Yi; Gherzi, Roberto; Ong, Shao-En; Chan, Edward L.; Raijmakers, Reinout; Pruijn, Ger J. M.; Stoecklin, Georg; Moroni, Christoph; Mann, Matthias; Karin, Michael. AU Binding Proteins Recruit the Exosome to Degrade ARE-Containing mRNAs. Cell. 2001-11-16, 107 (4). ISSN 0092-8674. PMID 11719186. doi:10.1016/S0092-8674(01)00578-5 (英语).
- ^ Koonin, Eugene V.; Wolf, Yuri I.; Aravind, L. Prediction of the Archaeal Exosome and Its Connections with the Proteasome and the Translation and Transcription Machineries by a Comparative-Genomic Approach. Genome Research. 2001-02-01, 11 (2) [2022-08-02]. ISSN 1088-9051. PMC 311015
 . PMID 11157787. doi:10.1101/gr.162001. (原始内容存档于2022-06-15) (英语).
. PMID 11157787. doi:10.1101/gr.162001. (原始内容存档于2022-06-15) (英语).
- ^ Evguenieva‐Hackenberg, Elena; Walter, Pamela; Hochleitner, Elisabeth; Lottspeich, Friedrich; Klug, Gabriele. An exosome‐like complex in Sulfolobus solfataricus. EMBO reports. 2003-09, 4 (9) [2022-08-02]. ISSN 1469-221X. PMC 1326366
 . PMID 12947419. doi:10.1038/sj.embor.embor929. (原始内容存档于2019-04-26) (英语).
. PMID 12947419. doi:10.1038/sj.embor.embor929. (原始内容存档于2019-04-26) (英语).
- ^ 7.0 7.1 7.2 7.3 7.4 7.5 Schilders, Geurt; van Dijk, Erwin; Raijmakers, Reinout; Pruijn, Ger J.M. Cell and Molecular Biology of the Exosome: How to Make or Break an RNA. International Review of Cytology 251. Elsevier. 2006: 159–208 [2022-08-02]. ISBN 978-0-12-364655-2. doi:10.1016/s0074-7696(06)51005-8. (原始内容存档于2019-10-21) (英语).
- ^ Lorentzen, Esben; Walter, Pamela; Fribourg, Sebastien; Evguenieva-Hackenberg, Elena; Klug, Gabriele; Conti, Elena. The archaeal exosome core is a hexameric ring structure with three catalytic subunits. Nature Structural & Molecular Biology. 2005-07, 12 (7) [2022-08-02]. ISSN 1545-9985. doi:10.1038/nsmb952. (原始内容存档于2022-06-17) (英语).
- ^ 9.0 9.1 Shen, Vincent; Kiledjian, Megerditch. A View to a Kill: Structure of the RNA Exosome. Cell. 2006-12-15, 127 (6). ISSN 0092-8674. PMC 1986773
 . PMID 17174886. doi:10.1016/j.cell.2006.11.035 (英语).
. PMID 17174886. doi:10.1016/j.cell.2006.11.035 (英语).
- ^ Raijmakers, Reinout; Egberts, Wilma Vree; van Venrooij, Walther J.; Pruijn, Ger J. M. Protein–Protein Interactions between Human Exosome Components Support the Assembly of RNase PH-type Subunits into a Six-membered PNPase-like Ring. Journal of Molecular Biology. 2002-11-01, 323 (4). ISSN 0022-2836. doi:10.1016/S0022-2836(02)00947-6 (英语).
- ^ Walter, Pamela; Klein, Franziska; Lorentzen, Esben; Ilchmann, Anne; Klug, Gabriele; Evguenieva-Hackenberg, Elena. Characterization of native and reconstituted exosome complexes from the hyperthermophilic archaeon Sulfolobus solfataricus. Molecular Microbiology. 2006-11, 62 (4) [2022-08-02]. ISSN 0950-382X. doi:10.1111/j.1365-2958.2006.05393.x. (原始内容存档于2022-03-21) (英语).
- ^ Ishii, Ryohei; Nureki, Osamu; Yokoyama, Shigeyuki. Crystal Structure of the tRNA Processing Enzyme RNase PH from Aquifex aeolicus *. Journal of Biological Chemistry. 2003-08-22, 278 (34). ISSN 0021-9258. PMID 12746447. doi:10.1074/jbc.M300639200 (英语).
- ^ Harlow, L. S. Crystal structure of the phosphorolytic exoribonuclease RNase PH from Bacillus subtilis and implications for its quaternary structure and tRNA binding. Protein Science. 2004-02-06, 13 (3). ISSN 0961-8368. PMC 2286726
 . PMID 14767080. doi:10.1110/ps.03477004 (英语).
. PMID 14767080. doi:10.1110/ps.03477004 (英语).
- ^ Symmons, Martyn F.; Jones, George H.; Luisi, Ben F. A Duplicated Fold Is the Structural Basis for Polynucleotide Phosphorylase Catalytic Activity, Processivity, and Regulation. Structure. 2000-11-15, 8 (11) [2022-08-02]. ISSN 0969-2126. PMID 11080643. doi:10.1016/S0969-2126(00)00521-9. (原始内容存档于2013-06-26) (英语).
- ^ Lin-Chao, Sue; Chiou, Ni-Ting; Schuster, Gadi. The PNPase, exosome and RNA helicases as the building components of evolutionarily-conserved RNA degradation machines. Journal of Biomedical Science. 2007-07, 14 (4). ISSN 1021-7770. doi:10.1007/s11373-007-9178-y (英语).
- ^ Schneider, Claudia; Anderson, James T.; Tollervey, David. The Exosome Subunit Rrp44 Plays a Direct Role in RNA Substrate Recognition. Molecular Cell. 2007-07-20, 27 (2). ISSN 1097-2765. PMC 7610968
 . PMID 17643380. doi:10.1016/j.molcel.2007.06.006 (英语).
. PMID 17643380. doi:10.1016/j.molcel.2007.06.006 (英语).
- ^ Mian, I. Comparative sequence analysis of ribonucleases HII, III, II PH and D. Nucleic Acids Research. 1997-08-15, 25 (16) [2022-08-02]. PMC 146874
 . PMID 9241229. doi:10.1093/nar/25.16.3187. (原始内容存档于2022-06-16).
. PMID 9241229. doi:10.1093/nar/25.16.3187. (原始内容存档于2022-06-16).
- ^ Raijmakers, Reinout; Schilders, Geurt; Pruijn, Ger J. M. The exosome, a molecular machine for controlled RNA degradation in both nucleus and cytoplasm. European Journal of Cell Biology. 2004-01-01, 83 (5). ISSN 0171-9335. doi:10.1078/0171-9335-00385 (英语).
- ^ Wang, Lingna; Lewis, Marc S.; Johnson, Arlen W. Domain interactions within the Ski2/3/8 complex and between the Ski complex and Ski7p. RNA. 2005-08-01, 11 (8) [2022-08-02]. ISSN 1355-8382. PMC 1370812
 . PMID 16043509. doi:10.1261/rna.2060405. (原始内容存档于2022-06-16) (英语).
. PMID 16043509. doi:10.1261/rna.2060405. (原始内容存档于2022-06-16) (英语).
- ^ LaCava, John; Houseley, Jonathan; Saveanu, Cosmin; Petfalski, Elisabeth; Thompson, Elizabeth; Jacquier, Alain; Tollervey, David. RNA Degradation by the Exosome Is Promoted by a Nuclear Polyadenylation Complex. Cell. 2005-06-03, 121 (5). ISSN 0092-8674. PMID 15935758. doi:10.1016/j.cell.2005.04.029 (英语).
- ^ 21.0 21.1 Liu, Quansheng; Greimann, Jaclyn C.; Lima, Christopher D. Reconstitution, Activities, and Structure of the Eukaryotic RNA Exosome. Cell. 2006-12-15, 127 (6). ISSN 0092-8674. PMID 17174896. doi:10.1016/j.cell.2006.10.037 (英语).
- ^ 22.0 22.1 Dziembowski, Andrzej; Lorentzen, Esben; Conti, Elena; Séraphin, Bertrand. A single subunit, Dis3, is essentially responsible for yeast exosome core activity. Nature Structural & Molecular Biology. 2007-01, 14 (1) [2022-08-02]. ISSN 1545-9985. doi:10.1038/nsmb1184. (原始内容存档于2022-06-17) (英语).
- ^ Lorentzen, Esben; Conti, Elena. Structural Basis of 3′ End RNA Recognition and Exoribonucleolytic Cleavage by an Exosome RNase PH Core. Molecular Cell. 2005-11-11, 20 (3). ISSN 1097-2765. PMID 16285928. doi:10.1016/j.molcel.2005.10.020 (英语).
- ^ Lejeune, Fabrice; Li, Xiaojie; Maquat, Lynne E. Nonsense-Mediated mRNA Decay in Mammalian Cells Involves Decapping, Deadenylating, and Exonucleolytic Activities. Molecular Cell. 2003-09-01, 12 (3). ISSN 1097-2765. PMID 14527413. doi:10.1016/S1097-2765(03)00349-6 (英语).
- ^ Wilson, Marenda A; Meaux, Stacie; van Hoof, Ambro. A Genomic Screen in Yeast Reveals Novel Aspects of Nonstop mRNA Metabolism. Genetics. 2007-10-01, 177 (2) [2022-08-02]. ISSN 1943-2631. PMC 2034642
 . PMID 17660569. doi:10.1534/genetics.107.073205. (原始内容存档于2022-07-27) (英语).
. PMID 17660569. doi:10.1534/genetics.107.073205. (原始内容存档于2022-07-27) (英语).
- ^ Lin, Wei-Jye; Duffy, Aaron; Chen, Ching-Yi. Localization of AU-rich Element-containing mRNA in Cytoplasmic Granules Containing Exosome Subunits *. Journal of Biological Chemistry. 2007-07-06, 282 (27). ISSN 0021-9258. PMID 17470429. doi:10.1074/jbc.M702281200 (英语).
- ^ 27.0 27.1 Allmang, C. Functions of the exosome in rRNA, snoRNA and snRNA synthesis. The EMBO Journal. 1999-10-01, 18 (19). PMC 1171609
 . PMID 10508172. doi:10.1093/emboj/18.19.5399.
. PMID 10508172. doi:10.1093/emboj/18.19.5399.
- ^ Schilders, G. MPP6 is an exosome-associated RNA-binding protein involved in 5.8S rRNA maturation. Nucleic Acids Research. 2005-11-27, 33 (21) [2022-08-02]. ISSN 0305-1048. PMC 1310903
 . PMID 16396833. doi:10.1093/nar/gki982. (原始内容存档于2022-01-21) (英语).
. PMID 16396833. doi:10.1093/nar/gki982. (原始内容存档于2022-01-21) (英语).
- ^ van Dijk, Erwin L.; Schilders, Geurt; Pruijn, Ger J.M. Human cell growth requires a functional cytoplasmic exosome, which is involved in various mRNA decay pathways. RNA. 2007-07, 13 (7). ISSN 1355-8382. PMC 1894934
 . PMID 17545563. doi:10.1261/rna.575107 (英语).
. PMID 17545563. doi:10.1261/rna.575107 (英语).
- ^ Carpousis, A. J. The Escherichia coli RNA degradosome: structure, function and relationship in other ribonucleolytic multienzyme complexes. Biochemical Society Transactions. 2002-04, 30 (2) [2022-08-02]. ISSN 0300-5127. PMID 12035760. (原始内容存档于2022-06-15).
- ^ Pope, Janet E. Scleroderma overlap syndromes. Current Opinion in Rheumatology. 2002-11, 14 (6) [2022-08-02]. ISSN 1040-8711. doi:10.1097/00002281-200211000-00013. (原始内容存档于2020-11-28) (美国英语).
- ^ Gelpi, C; Algueró, A; Martinez, M Angeles; Vidal, S; Juarez, C; Rodriguez-Sanchez, J L. Identification of protein components reactive with anti-PM/Scl autoantibodies. Clinical and Experimental Immunology. 2008-06-28, 81 (1). ISSN 1365-2249. PMC 1535032
 . PMID 2199097. doi:10.1111/j.1365-2249.1990.tb05291.x (英语).
. PMID 2199097. doi:10.1111/j.1365-2249.1990.tb05291.x (英语).
- ^ Targoff, Ira N.; Reichlin, Morris. Nucleolar localization of the PM-Scl antigen. Arthritis & Rheumatism. 1985-02, 28 (2) [2022-08-02]. doi:10.1002/art.1780280221. (原始内容存档于2022-03-21) (英语).
- ^ Raijmakers, Reinout; Renz, Manfred; Wiemann, Claudia; Egberts, Wilma Vree; Seelig, Hans Peter; van Venrooij, Walther J.; Pruijn, Ger J. M. PM-Scl-75 is the main autoantigen in patients with the polymyositis/scleroderma overlap syndrome. Arthritis & Rheumatism. 2004-02, 50 (2). ISSN 0004-3591. doi:10.1002/art.20056 (英语).
- ^ Brouwer, Rick; Vree Egberts, Wilma TM; Hengstman, Gerald JD; Raijmakers, Reinout; van Engelen, Baziel GM; Peter Seelig, Hans; Renz, Manfred; Mierau, Rudolf; Genth, Ekkehard; Pruijn, Ger JM; van Venrooij, Walther J. Autoantibodies directed to novel components of the PM/Scl complex, the human exosome. Arthritis Research & Therapy. 2001-11-12, 4 (2) [2022-08-02]. ISSN 1478-6362. PMC 83843
 . PMID 11879549. doi:10.1186/ar389. (原始内容存档于2022-03-21).
. PMID 11879549. doi:10.1186/ar389. (原始内容存档于2022-03-21).
- ^ Schilders, Geurt; Egberts, Wilma Vree; Raijmakers, Reinout; Pruijn, Ger J. M. C1D is a major autoantibody target in patients with the polymyositis–scleroderma overlap syndrome. Arthritis & Rheumatism. 2007-07, 56 (7). doi:10.1002/art.22710 (英语).
- ^ Mahler, Michael; Raijmakers, Reinout; Dähnrich, Cornelia; Blüthner, Martin; Fritzler, Marvin J. Clinical evaluation of autoantibodies to a novel PM/Scl peptide antigen. Arthritis Research & Therapy. 2005, 7 (3) [2022-08-02]. ISSN 1478-6362. PMC 1174964
 . PMID 15899056. doi:10.1186/ar1729. (原始内容存档于2022-03-21).
. PMID 15899056. doi:10.1186/ar1729. (原始内容存档于2022-03-21).
- ^ Mahler, Michael; Raijmakers, Reinout. Novel aspects of autoantibodies to the PM/Scl complex: Clinical, genetic and diagnostic insights. Autoimmunity Reviews. 2007-08-01, 6 (7). ISSN 1568-9972. doi:10.1016/j.autrev.2007.01.013 (英语).
- ^ Jablonska, S.; Blaszcyk, M. Scleromyositis: a scleroderma/polymyositis overlap syndrome. Clinical Rheumatology. 1998-11, 17 (6). ISSN 0770-3198. doi:10.1007/BF01451281 (英语).
- ^ Lum, Pek Yee; Armour, Christopher D.; Stepaniants, Sergey B.; Cavet, Guy; Wolf, Maria K.; Butler, J. Scott; Hinshaw, Jerald C.; Garnier, Philippe; Prestwich, Glenn D.; Leonardson, Amy; Garrett-Engele, Philip. Discovering Modes of Action for Therapeutic Compounds Using a Genome-Wide Screen of Yeast Heterozygotes. Cell. 2004-01-09, 116 (1). ISSN 0092-8674. PMID 14718172. doi:10.1016/S0092-8674(03)01035-3 (英语).
延伸阅读
[编辑]- Vanacova, Stepanka; Stefl, Richard. The exosome and RNA quality control in the nucleus. EMBO reports. 2007-07, 8 (7). ISSN 1469-221X. PMC 1905902
 . PMID 17603538. doi:10.1038/sj.embor.7401005 (英语).
. PMID 17603538. doi:10.1038/sj.embor.7401005 (英语). - Houseley, Jonathan; LaCava, John; Tollervey, David. RNA-quality control by the exosome. Nature Reviews Molecular Cell Biology. 2006-07, 7 (7) [2022-08-02]. ISSN 1471-0080. doi:10.1038/nrm1964. (原始内容存档于2022-06-12) (英语).
- Buttner, Katharina; Wenig, Katja; Hopfner, Karl-Peter. The exosome: a macromolecular cage for controlled RNA degradation. Molecular Microbiology. 2006-09, 61 (6) [2022-08-02]. ISSN 0950-382X. doi:10.1111/j.1365-2958.2006.05331.x. (原始内容存档于2022-06-07) (英语).
- Lorentzen, Esben; Conti, Elena. The Exosome and the Proteasome: Nano-Compartments for Degradation. Cell. 2006-05-19, 125 (4). ISSN 0092-8674. PMID 16713559. doi:10.1016/j.cell.2006.05.002 (英语).
- Pruijn, Ger J. M. Doughnuts dealing with RNA. Nature Structural & Molecular Biology. 2005-07, 12 (7) [2022-08-02]. ISSN 1545-9985. doi:10.1038/nsmb0705-562. (原始内容存档于2022-06-07) (英语).
- 王树启; 王金发. 外切体研究进展. 生物化学与生物物理进展. 2002, 29 (1): 10–13.
外部链接
[编辑]- (英文)蛋白质数据库中人源外切酶体的结构 (页面存档备份,存于互联网档案馆)
- (英文)蛋白质数据库中古菌外切酶体的结构 (页面存档备份,存于互联网档案馆)
- (英文)蛋白质数据库中古菌外切酶体与RNA结合的结构 (页面存档备份,存于互联网档案馆)
- (英文)蛋白质数据库中酵母外切酶体亚基Rrp6的结构 (页面存档备份,存于互联网档案馆)
