磷唑
外观
| 磷唑 | |||
|---|---|---|---|
| |||
| IUPAC名 1H-Phosphole[1] | |||
| 别名 | 磷杂茂、磷杂环戊二烯 | ||
| 识别 | |||
| CAS号 | 288-01-7 | ||
| PubChem | 164575 | ||
| ChemSpider | 144273 | ||
| SMILES |
| ||
| InChI |
| ||
| 性质 | |||
| 化学式 | C4H5P | ||
| 摩尔质量 | 84.06 g·mol−1 | ||
| 相关物质 | |||
| 相关含磷杂环 | 三磷唑 五磷唑 | ||
| 相关化学品 | 吡咯 铋唑 砷唑 锑唑 磷杂苯 | ||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
磷唑是一种有机磷化合物,化学式 C
4H
4PH,是吡咯的磷衍生物。
结构和成键
[编辑]不像相关的五元杂环化合物——吡咯、噻吩和呋喃,磷唑衍生物的芳香性被减弱,反映了磷不愿意使它的孤对电子变成离域电子。[2]这种差异的主要标志是磷原子的锥体化(从平面三角形构型变成三角锥构型)。磷唑的反应性也表明了它没有芳香性。[3]磷唑衍生物会经历不同的环加成反应,它们的配位特性也得到了很好的研究。[4]
制备
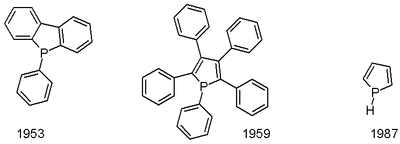
[编辑]磷唑是在1987年发现的,[5]是由磷唑锂(C4H4PLi)在低温下质子化而成的。[6]磷唑的衍生物可以通过涉及1,3-二烯加成到二氯烃基磷(RPCl2)的麦克马考反应,然后脱卤反应而成。[7]
反应性
[编辑]磷唑中的P-H键支配了此类化合物的反应性。[6]磷唑母体很容易发生重排反应,会把氢原子从磷迁移到2号碳,然后二聚。
很多磷唑的衍生物中的磷都和另一个烃基键结,这个烃基通常是甲基或苯基。磷唑衍生物的非芳香性表现在它们的反应性上,但P-C键仍然保持完整。举个例子,它们会和亲电性的炔烃发生狄尔斯–阿尔德反应。磷唑衍生物的磷原子呈碱性,可作为配体。[6]
参见
[编辑]参考资料
[编辑]- ^ Nomenclature of Organic Chemistry: IUPAC Recommendations and Preferred Names 2013 (Blue Book). Cambridge: The Royal Society of Chemistry. 2014: 146. ISBN 978-0-85404-182-4. doi:10.1039/9781849733069-00130.
- ^ D. B. Chesnut; L. D. Quin. The important role of the phosphorus lone pair in phosphole aromaticity. Heteroatom Chemistry. 2007, 18: 754. doi:10.1002/hc.20364.
- ^ Philip Hindenberg; Carlos Romero-Nieto. Phosphaphenalenes: An Evolution of the Phosphorus Heterocycles. Synlett. 2016, 27: 2293–2300. doi:10.1055/s-0035-1562506.
- ^ Almaz Zagidullin; Vasily A. Miluykov. Phospholes – development and recent advances. Mendeleev Communications. 2013, 23: 117–130. doi:10.1016/j.mencom.2013.05.001.
- ^ P. J. Fagan, W. A. Nugent (1992). "1-Phenyl-2,3,4,5-tetramethylphosphole". Org. Synth.; Coll. Vol. 9: 653.
- ^ 6.0 6.1 6.2 Claude Charrier; Hubert Bonnard; Guillaume De Lauzon; Francois Mathey. Proton [1,5] shifts in P-unsubstituted 1H-phospholes. Synthesis and chemistry of 2H-phosphole dimers. J. Am. Chem. Soc. 1983, 105: 6871–6877. doi:10.1021/ja00361a022.
- ^ W. B. McCormack (1973). "3-Methyl-1-Phenylphospholene oxide". Org. Synth.; Coll. Vol. 5: 787.