氯酸钾
外观
| 氯酸钾 | |
|---|---|

| |
| |

| |
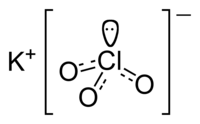
| IUPAC名 Potassium Chlorate | |
| 识别 | |
| CAS号 | 3811-04-9 |
| PubChem | 6426889 |
| ChemSpider | 18512 |
| SMILES |
|
| InChI |
|
| InChIKey | VKJKEPKFPUWCAS-REWHXWOFAC |
| UN编号 | 1485 |
| EINECS | 223-289-7 |
| RTECS | FO0350000 |
| 性质 | |
| 化学式 | KClO3 |
| 摩尔质量 | 122.55 g·mol⁻¹ |
| 外观 | 无色透明结晶或白色粉末 |
| 密度 | 2.32 g/cm3 (固) |
| 熔点 | 356 °C |
| 沸点 | ~400 °C 分解 |
| 溶解性(水) | 7.3 g/100 ml (20 °C) (70F) |
| 溶解性(甘油) | 2 g/100 mL[1] |
| 危险性 | |
GHS危险性符号   [2] [2]
| |
| GHS提示词 | Danger |
| H-术语 | H271, H302, H332, H411[2] |
| P-术语 | P220, P273[2] |
| NFPA 704 | |
| 闪点 | 无 |
| 相关物质 | |
| 其他阴离子 | 溴酸钾、碘酸钾 |
| 其他阳离子 | 氯酸铵 氯酸锂 氯酸钠 氯酸铷 氯酸铯 |
| 相关化学品 | 氯化钾、次氯酸钾 亚氯酸钾、高氯酸钾 |
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |
氯酸钾由钾、氯和氧元素组成,化学式为KClO3。它在室温时是无色晶体或白色粉末,而且是一种强氧化剂,可溶于水和甘油,不溶于醇。其折光率为1.5167[1]。有毒,口服5~10克可致死。[3]
制备
[编辑]- 氯酸钾在工业上属于氯碱工业的产品。通过电解热食盐水得到氯酸钠,然后与氯化钾发生复分解反应。溶解度小的氯酸钾即可沉淀出来。用重结晶的方法加以提纯。此外,工业上也会用热的石灰乳和氯气反应,再和氯化钾复分解,得到氯酸钾[4]。
其他制备方法
[编辑]氯酸钾也能通过将氯气通入热的氢氧化钾溶液的方法来制备[5]:
用途
[编辑]氯酸钾是传统火药的主要成分,这个成分用到现在都未完全被高氯酸钾取代。
氯酸盐系的化学物品因为不易潮解,一直受到火药制造者的欢迎。然而,氯酸盐与硫、磷等强还原剂会形成不稳定的爆炸性混合物。因此,氯酸盐系需于特别设计的设备中使用[来源请求]。氯酸钾与铝粉的混合物在密闭体系中爆燃可以产生特别的音效,因此被用作爆竹中的爆鸣剂。
作为一种强氧化剂,氯酸钾可以与许多还原剂形成爆炸性混合物,亦被用于调节某些炸药的氧平衡,籍以改善其性能。在第一次世界大战时,曾出现以塑化剂(e.g.:聚异丁烯)和氯酸钾为主要成分的塑性炸药,并被用于手榴弹内。不少的火药都以氯酸钾取代爆炸性较弱的硝酸钾。
化学性质
[编辑]氯酸钾与催化剂二氧化锰()进行混合加热到200℃,可以释放出氧气与氯化钾。这种方法是一种常见的实验室制氧法。
其化学反应为:
在酸性溶液中,氯酸盐会被Cl-还原为二氧化氯[6]。氯酸盐也能在酸性条件下和Br-、I-反应,得到相应的单质Br2和I2[7]。
潜在危险
[编辑]
由于氯酸钾与硫、磷、碳等还原性物质混合后,经摩擦或撞击后就会发生燃烧或爆燃[8],甚至有自发反应的可能性,所以需小心处理,含氯酸钾的火药就要避免和硫磺接触,否则会出现猛烈爆燃[来源请求]。
氯酸钾能使血红蛋白变性并分解,误食会引起急性中毒,致死量为10g[9]。
参考资料
[编辑]- ^ 1.0 1.1 J.A.迪安. 兰氏化学手册. 科学出版社. 1991: P331. ISBN 7-03-000840-5.
- ^ 2.0 2.1 2.2 Potassium chlorate. [14 February 2022]. (原始内容存档于2012-09-22).
- ^ ICSC 0548 化学品安全说明书. 2009-09-06 [2010-04-20]. (原始内容存档于2006-04-13).
- ^ Реми, Г. Курс неорганической химиию, т. 1/Перевод с немецкого под ред. А. В. Новосёловой. Москва:Мир, 1972.- с. 770//(translated from:) Heinrich Remy. Lehrbuch der anorganischen Chemie. XI Auflage. Band 1. Leipzig:Geest & Portig K.-G., 1960.
- ^ 5.0 5.1 Pradyot Patnaik. Handbook of Inorganic Chemicals. McGraw-Hill, 2002, ISBN 978-0-07-049439-8
- ^ 《无机化学》丛书(张青莲 主编).第六卷 卤素、铜分族、锌分族.2.6.4 卤素含氧酸及其盐.P293
- ^ 《无机化学》丛书(张青莲 主编).第六卷 卤素、铜分族、锌分族.2.6.4 卤素含氧酸及其盐.P315
- ^ 高等教育出版社. 无机化学. 第四版. 2010: P295. ISBN 978-7-04-028478-2.
- ^ 高等教育出版社. 无机化学. 第四版. 2010: P296. ISBN 978-7-04-028478-2.




![{\displaystyle {\rm {\ 2KClO_{3}{\xrightarrow[{\Delta }]{MnO_{2}}}3O_{2}\uparrow +2KCl}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/25826e01809c29fe70b6b028afa70b780d7bf4b6)
