薄層色譜法
 黑墨水在TLC板上的分離 | |
| 英文縮寫 | TLC |
|---|---|
| 分類 | 層析法 |
| 其它技術 | |
| 其它技術 | 瓊脂糖凝膠電泳 SDS-PAGE |
薄層色譜法(英語:Thin layer chromatography,簡稱TLC,又稱為薄層色譜法)是一種用於分離混合物的層析技術。[1] 在分析化學特別是針對有機化合物的分析中,薄層層析是極為重要的分離方法。
薄層層析在覆蓋有很薄一層吸附劑的玻璃板、塑料片或鋁箔上進行。吸附劑又稱為薄層色譜固定相:常為硅膠、氧化鋁或纖維素。操作時先將待分離樣品用毛細管點於板上,然後在密閉的層析缸中,用單一或混合溶劑作為流動相,由流動相的毛細作用緩慢地將混合物樣品中的不同組分由下而上爬升至板的頂端。因為樣品中各組分與固定相的作用力不同,在流動相中溶解度也不同,導致各組分的上升速度有差異而最終在板上形成上下不一的斑點,從而達到分離混合物的目的。[2]
薄層層析在監測反應進程,鑑定特定化合物以及測定物質的純度等均有廣泛的應用,如:分析神經醯胺與脂肪酸;檢測在食物和水中的農藥或殺蟲劑;在法醫的工作中,分析纖維的染料成份;化驗放射性藥物的放化純度;鑑定藥用植物及分析其內部成分。[3]
高效薄層色譜是對經典薄層色譜的改進法之一,該法中色譜的靈敏度和分離度都有很大的提高,可以準確地檢出極微量的物質。
薄層板的製作
[編輯]市面上根據薄層層析板(如硅膠G板或聚酰胺板)的固定相標準顆粒大小分為不同規格,通常顆粒越細分離效果越好。製作時首先將吸附相(如硅膠)與少量惰性粘合劑(如硫酸鈣)和水混合形成的漿狀物,均勻地鋪於以玻璃片、厚鋁箔或塑料製成的載板上。鋪過固定相的板先晾乾,然後在烤爐內於110℃加熱三十分鐘進行活化。用於分析鑒定時吸附劑厚度一般為0.1–0.25毫米,而用於製備時(見下文)則為0.5–2.0毫米。[4]
薄層層析技術
[編輯]
薄層層析的操作過程類似於紙色譜法,原理方面類似於柱色譜,因而與紙色譜相比具有很多優勢,如它分離效果好,靈敏快速,對於固定相的選擇更多,且TLC的結果還可作為柱層析的參考。由於以上的諸多優勢,使薄層層析技術成為當今檢測化學反應、定性分析化合物和分離化合物的最常用的手段。實驗室常用的是硅膠薄層層析,其製作簡單、成本低廉且用途廣泛。在化學技術當中,符合這幾點的技術方法並不多見。
分離的過程與原理
[編輯]在混合物中,不同化合物會以不同的速率前進,其原因為吸引力及固定相的差異和樣本溶質在溶劑裡溶解度的差異[5]。樣本的分離(以Rf值來比較)結果是可以藉由改變洗脫溶劑或使用的混合的洗脫溶劑來改變的。化合物的分離是利用化合物與流動相之間在固定相上競爭結合位所造成的。例如:使用矽膠做為固定相的話,此固定相可以被視為極性。此時加入兩不同極性的化合物,極性較強的化合物與矽膠間會有較強作用力,因此,更能抵抗流動相並與矽膠結合;極性較弱的化合物與矽膠的作用能力較差,因此更容易流動,擁有更高的Rf值[5]。如果流動相的極性變得更強的話,這樣更能夠抵抗化合物與膠上結合的能力,使所有TLC片上的化合物上升到更高的位置。這樣的溶劑我們稱為「強」溶劑(洗脫劑),而「弱」洗脫劑則幾乎不能移動它們。「強」與「弱」的比較是取決於TLC片上的塗層(固定相)。以矽膠TLC片來說,洗脫劑的強度比較為:
全氟烷(最弱)<己烷<戊烷<四氯化碳<苯/甲苯<二氯甲烷<乙醚<乙酸乙酯<乙腈<丙酮<丙醇/正丁醇<水<甲醇<三乙胺<乙酸<甲酸(最強)
C18的相位與TLC相反。在應用上,使用乙酸乙酯和己烷的混合物做為流動相的話,加入更多的乙酸乙酯會使TLC片上所有化合物的Rf値升高。改變流動相的極性通常並不會使TLC片上的化合物的前後順序發生改變。如果要使化合物的前後順序發生改變的話,此時就應使用非極性的固定相來代替極性固定相,如C18-官能基矽膠。
操作
[編輯]薄層色譜的步驟如下:[6]
- 點樣:將試樣溶液用毛細管在層析板上距離板底部約1.5厘米的位置點若干下(次數根據樣品濃度而定),並靜置頃刻(或加熱)以使溶劑完全蒸發。若溶劑難以揮發,則點樣之後需要將板放於真空容器中乾燥後再使用。溶劑的蒸發是必須的,否則殘留的溶劑會與流動相作用,降低流動相的均一性,導致分離效果變差。
- 將少量合適的溶劑(流動相)倒於一個合適的玻璃器皿(展缸)中,讓流動相高度不超過1厘米,並在上面放上表面皿使溶劑蒸氣在展缸中飽和。可在展缸底部放上一張濾紙,讓濾紙底部浸沒於溶劑中並靠在展缸內壁,過幾分鐘後讓洗脫溶劑蒸發並在展缸空間內飽和。若不經過以上步驟可能會導致分離度的下降或使結果不具重複性。
- 然後將層析板置於展缸內(樣品點不可觸碰溶劑表面),蓋上蓋子讓溶劑通過毛細現象緩慢爬升。溶劑遇到樣品混合點時,會帶着樣品上升(即洗脫樣品)。當溶劑快到層析板頂端時,將板拿出,迅速記錄溶劑到達的高度並晾乾。不要讓溶劑爬升到達板的頂部。
Rf值 (retention factor)
[編輯]對於確定的固定相,混合物樣品中不同的化合物在層析板上爬升的速度不同,這是由於它們對於固定相的吸附能力不同,對於洗脫劑的溶解能力也不同。改變不同的洗脫溶劑,或用不同溶劑配成混合洗脫劑,化合物的分離效果可自行調節。組分在板上的分離情況一般用比移值(Rf)的大小來表徵。薄層色譜板上的分離情況還可用於預測柱色譜法或快速柱色譜法的分離效果。[7]
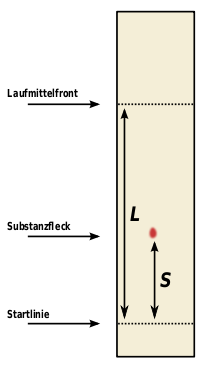
Startlinie = 樣品的起始線
Substanzfleck = 樣品中某成份的顯色點
Laufmittelfront = 溶劑到達的位置
由於薄層色譜中很難產生均勻的吸附劑塗層,且薄板的質量與吸潮程度亦參差不齊,所以即便是同一物質在同類型而不同的層析板上得到的比移值也難以完全一致。相比於紙色譜這是薄層色譜的缺點。操作中常常將標準試樣與試樣在同一薄板上同時展開並點上混合點,以克服這一缺點。
化合物的分離是利用化合物與流動相之間在固定相上競爭結合位所造成的。例如:使用矽膠做為固定相的話,此固定相可以被視為極性。此時加入兩不同極性的化合物,極性較強的化合物與矽膠間會有較強作用力,因此,更能抵抗流動相並與矽膠結合;極性較弱的化合物與矽膠的作用能力較差,因此更容易流動,擁有更高的Rf値。如果流動相的極性變得更強的話,這樣更能夠抵抗化合物與膠上結合的能力,使所有TLC片上的化合物上升到更高的位置。這樣的溶劑我們稱為"強"溶劑(洗脫劑),而"弱"洗脫劑則幾乎不能移動它們。"強"與"弱"的比較是取決於TLC片上的塗層(固定相)。
洗脫劑(流動相)
[編輯]以矽膠TLC片來說,洗脫劑的強度比較為:
而對於C18覆蓋的TLC板,其順序完全相反。在應用中,若使用乙酸乙酯/庚烷的混合溶劑作為流動相,乙酸乙酯比例越高會導致所有化合物在TLC上的Rf值更大。通常,更改流動相的極性不會導致TLC板上的化合物斑點前後順序發生改變。若需要更改化合物在TLC板上的前後順序,可以選用反相TLC板,即使用非極性固定相來代替極性固定相,如C18修飾後的硅膠。
製備TLC
[編輯]TLC還可用於少量如100毫克左右的化合物的分離,此時混合物樣品不是「點」在板上,而是塗抹在TLC板上且高於洗脫劑液面上的位置,形成一條水平的樣品帶。然後如同展開小型TLC板一樣將製備TLC板展開並晾乾,然後將每條攜帶不同化合物的色帶從板上分別刮下,並用合適的溶劑萃取洗滌(如二氯甲烷)並過濾掉固定相等不溶物,得到濾液後再脫除溶劑就得到純淨的化合物。對於小量且易於分離的反應產物,製備TLC較柱色譜法在時間、效率和經濟上更佔優勢。顯然,這種方法得到的TLC板不可用全部用化學方法顯色,否則會導致樣品全部損失。因此可使用一些不會破壞樣品的顯色方法,如紫外線。或者,可刮下板上部分的吸附相進行鑑定,也可以割下部分的TLC板用顯色劑(如碘)找到需要的化合物。
分析與顯色
[編輯]由於被分離出的化學品可能是無色的,因此下列幾種方法可用於讓沒有可見光吸收的斑點顯色:
- 通常在可使用少量的熒光化合物,如錳-活化的鋅硅酸鹽加入到吸附相當中,使得吸附物在黑光(UV254)下可以顯色。固定相在熒光下本身顯綠色,因此化合物的斑點可以掩蓋掉熒光下的綠色從而達到顯色目的。
- 碘蒸氣是對於大多數化合物都是顯色試劑
- 許多化合物的斑點可以通過將TLC板浸沒於下列顯色劑當中而達到顯色目的[8],如:高錳酸鉀,碘,溴,磷鉬酸,茴香醛法與茚三酮。
- 脂類的情況下,色譜圖可能會被轉移到PVDF膜上,然後受到進一步的分析,如質譜法,這種技術稱為Far-Eastern blotting。
當顯色成功後,就可以計算出Rf值,或保留因子。其計算方法是測量每個點從原點到達最終停留位置的距離除以原點到溶劑前沿的距離。這些值取決於使用的溶劑與TLC板的材質,而與物理常數無關。
應用與實例
[編輯]在有機化學中,有機反應可通過TLC進行定性的檢測。使用毛細管將樣品點於TLC板上:一個點表示起始原料,一個點表示反應體系,一個點表示兩者「混合點」。一個小型TLC板(3X7cm)只需幾分鐘就可以完全展開。整個分析過程是定性的,它可顯示起始原料是否消失即是否反應已經完成;是否有產物出現以及產生了多少產物。需注意的是,從低溫環境中取樣的TLC結果可能會出現誤差,因為樣品的溫度在毛細管中就已經升至室溫,其與低溫反應瓶內的反應將不一樣。例如DIBAL-H還原酯製備醛的反應。
以下是一個實例:使用薄層層析法分離綠葉的提取物(如菠菜)的7個階段。胡蘿蔔素洗脫的速度很快因此只能在第二步中看到。葉綠素A和B在最後一步的中間位置,葉黃素是保持黃色的第一個斑點。
-
第一步
-
第二步
-
第三步
-
第四步
-
第五步
-
第六步
-
第七步
參考文獻
[編輯]- ^ Laurence M. Harwood, Christopher J. Moody. Experimental organic chemistry: Principles and Practice Illustrated edition. WileyBlackwell. 13 Jun 1989: 159–173 790. ISBN 978-0632020171.
- ^ Vogel's Textbook of Practical Organic Chemistry (5th Edition) (Hardcover) by A.I. Vogel (Author), A.R. Tatchell (Author), B.S. Furnis (Author), A.J. Hannaford (Author), P.W.G. Smith ISBN 978-0-582-46236-6
- ^ Reich, E.; Schibli A. High-performance thin-layer chromatography for the analysis of medicinal plants (illustrated edition). Thieme: New York, 2007. ISBN 978-3-13-141601-8 (頁面存檔備份,存於網際網路檔案館)
- ^ Tables showing the thickness value of commercial regular and preparative Thin Layer Chromatography plates. [2011-05-20]. (原始內容存檔於2011-07-14).
- ^ 5.0 5.1 Thin Layer Chromatography (TLC): Principle with animation. [2013-02-08]. (原始內容存檔於2013-02-08).
- ^ Thin Layer Chromatography: How To. [2011-05-20]. (原始內容存檔於2017-11-25).
- ^ Fair, J. D.; Kormos, C. M. J. Chromatogr. A 2008, 1211(1-2), 49-54. (doi:10.1016/j.chroma.2008.09.085)
- ^ Thin Layer Chromatography stains. [2011-05-20]. (原始內容存檔於2011-07-15).






