工藝化學
工藝化學是開發與優化合成方案和工業生產流程的藥物化學分支,用於製造藥物開發階段所需要的化合物。其研究重點與主要負責在藥物研究早期階段中設計並較小規模地合成分子的藥物化學有所區別。
一般來說,藥物化學家主要專注於利用便於調節的化學構件中快速合成大量化合物(通常用於SAR研究)。而藥物發現化學中使用的反應庫一般較小(例如,Buchwald-Hartwig 胺化、Suzuki 偶聯和還原胺化等常見的反應)。 [1]工藝化學家的任務則是確定一種安全、成本低、勞動效率高、符合綠色化學理念、可重複性強,並綜合其他因素優化充分設計的化學工藝。通常,在尋找最短、最有效的合成路線時,工藝化學家必須設計創造性的合成解決方案,以減少高成本的官能基操作和氧化還原步驟。
本文只關注與小分子藥物生產相關的化學和製造過程。生物醫療產品(通常稱為「生物製劑」)的製造過程超出了本文的討論範圍。此外,與化工(例如傳熱和反應器設計)和藥物配方相關的許多複雜因素在本文中僅作粗略介紹。
工藝化學中的考慮因素
[編輯]成本效率在工藝化學中至關重要,是考慮試驗工廠合成路線的重點。在配製之前製造的藥物物質通常被稱為活性藥物成分(API)。API生產成本可分為兩部分:「材料成本」和「轉換成本」。 [2]合成過程的生態和環境影響也應通過適當的度量進行評估。
理想的工藝化學路線應當高度符合這些指標,但在實際上往往不可避免地需要權衡取捨。大多數大型製藥部門都設計了用於比較合成路線之間優劣的加權定量方案。由於成本是主要驅動因素,因此材料成本和體積時間產出通常占很大權重。
材料成本
[編輯]材料成本是從外部供應商處採購的所有原材料、中間體、試劑、溶劑和催化劑的成本總和。
轉換成本
[編輯]轉換成本是該過程在材料和時間方面的整體效率及其再現性的一個因素。化學過程的效率可以通過其原子經濟性、產量、體積時間輸出和環境因素(E-factor)來量化,其再現性可以通過質量服務水平(QSL)和過程卓越指數(PEI)來評估。

原子經濟性
[編輯]反應的原子經濟性定義為結合到最終產品中的起始材料的原子數。原子經濟可以看作給定合成路線「效率」的指標。 [3]
例如,Claisen 重排和Diels-Alder 環加成的原子經濟性為100%,而原型Wittig 反應的原子經濟性特別差(在所示示例中僅為20%)。
工藝合成路線的設計應使整個合成方案的原子經濟性達到最高。因此,在合成路線設計中應儘可能避免使用「昂貴」的試劑,例如保護基團和高分子量離去基團。API合成的原子經濟性值的理想範圍在70%~90%,但是對於某些較為複雜的目標分子,可能難以達到這樣的要求。然而,原子經濟性是比較合成同一分子的兩條路線優劣的重要指標。
產率
[編輯]產率定義為化學反應中獲得的產物的量。產量是否可接受完全取決於產品的重要性或是否有技術能夠使其發揮效用。定量指的是接近100%的產率,而高產率往往指高於90%的產率。 [4]
在工藝路線的設計中可以採用幾種策略來提高藥物產品的產率。首先是收斂性合成策略。假設每個合成步驟的收率都非常好,在後期組合幾個相互獨立製備的關鍵中間體可以最大化多步反應的總收率。
另一種提高產率(以及時間效率)的策略是一鍋合成法。這種方法是在一個反應器中使反應物連續進行多步反應,通常通過簡單地將試劑依次添加到反應器中。這樣可以避免在後處理過程中冗長的分離過程和中間體化合物的純化過程,從而節省時間與資源並且提高產率。
為了最大限度地降低總成本,涉及昂貴試劑、溶劑或催化劑的合成步驟應儘可能晚地引入到合成路線中,以最大限度地減少試劑用量。
在試驗工廠或製造工廠環境中,產率對API合成的材料成本有重大影響,因此規劃穩健路線與微調反應條件至關重要。選擇合成路線後,工藝化學家將對每個步驟進行詳盡的優化,以最大限度地提高總產量。低產率通常表明形成了不需要的副產物,需要在反應監控過程與反應器清潔過程中注意。
體積-時間輸出
[編輯]體積-時間輸出(VTO)代表特定過程或API合成的化學反應器佔用成本。高VTO表明特定合成步驟在用於給定輸出的「反應器小時數」方面成本很高。從數學上講,特定過程的VTO是通過佔用的所有反應器的總體積(m3)乘以每批次的小時數除以該批次的API或中間體的輸出(kg)得到的。
例如,勃林格殷格翰的工藝化學小組針對任何給定的合成步驟或化學過程的目標是VTO小於1。
此外,考慮了特定反應器的運營成本和可用容量後,可以從 VTO計算API合成的原始轉化成本。通常,對於大批量的API,建立專門工廠比使用試驗工廠更加經濟。
環境因子 (e-factor) 和過程質量強度 (PMI)
[編輯]這兩項指標可以體現合成反應對環境影響,旨在衡量製造過程中廢物處理的顯着且不斷上升的成本。整個 API 工藝的環境因子是通過合成方案中產生的廢物總質量與分離產品質量的比率來計算的。
與此類似,過程質量強度 (PMI) 計算原料總質量與分離產品質量的比率。
計算這兩個指標時,需要計入合成中使用的所有材料,包括反應和後處理溶劑、試劑和催化劑等。考慮了與外包中間體或通用試劑合成相關的廢物時,可能會出現環境因子或 PMI 計算的不一致。在此計算中忽略了產生的廢物對環境的影響。環境商 (EQ)則考慮了這一因素,它由環境因子乘以與各種廢物流相關的「不友好商」得出。單個合成步驟的環境因子或 PMI 的合理目標一般在10~40。
質量服務水平 (QSL)
[編輯]最後兩個「轉化成本因素」考慮的是給定反應或API合成路線的可重複性。質量服務水平 (QSL) 是對分離的中間體或最終API質量可重複性的衡量。本質上,QSL的計算涉及質量滿意的批次與總批次數的比率。合理的QSL目標值一般是 98%-100%。
過程卓越指數 (PEI)
[編輯]與QSL一樣,過程卓越指數 (PEI) 也是衡量過程再現性的指標。然而,在這裏,程序的穩健性是根據各種操作的產量和週期時間來評估的。PEI產量定義如下:
實際上,如果一個過程產率高,並且產率結果的分佈範圍窄,那麼PEI應該非常高。重現性差的過程可能是因為吸出率較高或平均產量較低,從而降低了PEI產量。
類似地,PEI循環時間可以定義如下:
這個表達式中以上項被取倒,以反映週期時間的優劣性。如果這些操作在製造工廠環境中是速度受限的,則關鍵過程(例如反應、離心或乾燥)循環時間的可重複性可能至關重要。如果一個分離步驟特別困難或緩慢,它可能成為API合成的瓶頸,在這種情況下,該操作的重現性和優化至關重要。
對於API製造過程,所有PEI指標(產量和週期時間)的目標一般都在98%-100%。
生態尺度影響指標
[編輯]2006 年,范阿肯等人[5]開發了一個定量框架來評估化學過程的安全性和生態影響,此外,該定量框架還加入了對實際情況和經濟因素的一定考慮,但權重較小。後人通過添加、減小、調整各種指標的權重來修改這個指標。除其他因素外,生態尺度影響指標還考慮了所用試劑的毒性、可燃性和爆炸穩定性、任何非標準或潛在危險的反應條件(例如,高壓或惰性氣氛)以及反應溫度。一些生態尺度影響指標與之前考慮的標準(例如環境因子)有所重複。
綜合案例研究
[編輯]勃林格殷格翰 HCV 蛋白酶抑制劑 (BI 201302)
[編輯]大環合成是工藝化學家經常面臨的挑戰。該領域有一個富有意義的案例:用於治療丙型肝炎的新型NS3蛋白酶抑制劑的合成。[6]勃林格殷格翰的工藝化學團隊當時的任務是開發一種更便宜、更有效的方法來製備活性NS3抑制劑BI 201302與BILN 2061的類似物。BILN 2061的放大化合成路線在最初時存在兩個重大缺陷(如下圖所示)。[7]大環化步驟對交叉複分解反應存在四個固有挑戰:
- 通常需要高度稀釋以防止二烯原料發生聚合。然而,在試驗工廠環境中,高度稀釋導致反應的產量低、溶劑成本高、廢物處理成本高。
- 烯烴的關環複分解需要高催化劑負載量。由於該案例所使用的釕催化劑(第一代Hoveyda 催化劑)成本很高,因此高催化劑負載量在經濟上不可行。催化劑的再循環雖然也有探索,但實驗證明並不可行。
- 由於所選催化劑在反應動力學上較緩慢,該反應需要較長的反應時間。理論上,這種限制可以通過使用活性更強的催化劑來克服。然而,雖然第二代 Hoveyda 和 Grubbs 催化劑在動力學上比第一代催化劑活性高,但使用這些催化劑時反應生成了大量聚合產物。
- 交叉複分解反應條件下存在差向異構風險。勃林格殷格翰的工藝化學團隊進行了廣泛的機理研究。研究表明,差向異構化很可能通過釕環戊烯中間體發生。[8]與Grubbs 催化劑相比,該方案中使用的 Hoveyda 催化劑造成差向異構化的風險更小。
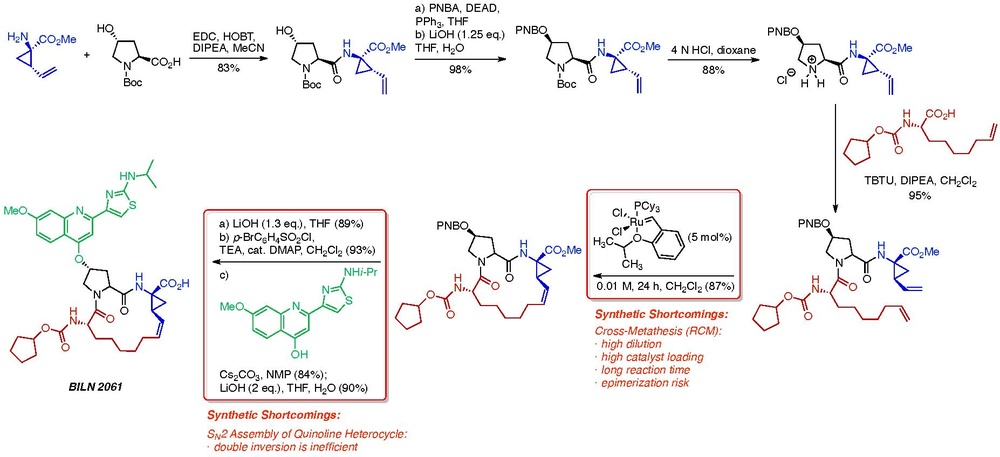
對交叉複分解反應的分析表明,無環前體的構象對聚合物形成有重要影響。勃林格殷格翰的化學家將C-4酰胺氮用Boc保護,把合成的起始部分由乙烯基環丙烷部分改為壬烯酸部分,提高了分子內反應的速率並降低了差向異構化的風險。此外,該反應所使用的催化劑從昂貴的第一代Hoveyda催化劑換為了更具反應性、更便宜的Grela催化劑。[9]改進後,競爭性聚合反應的速率顯著降低,使得合成能夠在0.1-0.2 M 的常規濃度下進行。
此外,該工藝化學團隊還設計了一種SNAr策略來連接喹啉雜環。改進後,羥脯氨酸部分的C-4位置的立體化學無需發生改變,避免了雙重SN2帶來的產率損失。 [10]
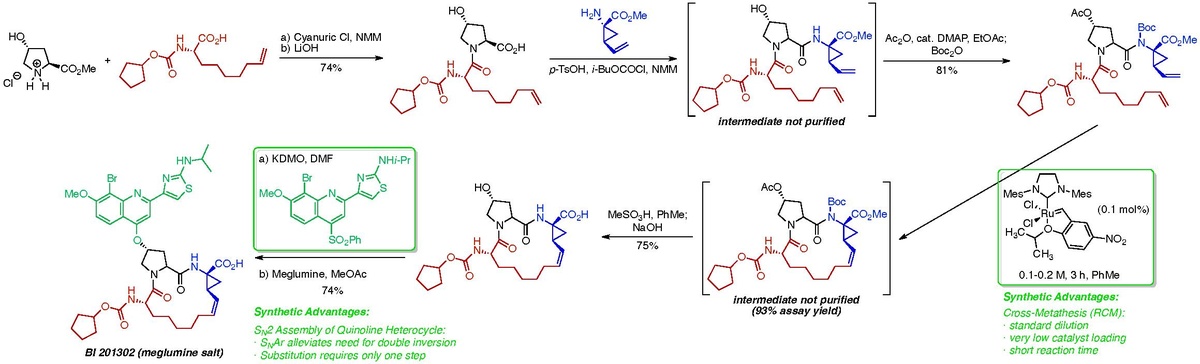
就VTO角度而言,在0.01 M 二烯濃度下使用Grela 催化劑按照未優化的方案進行交叉複分解反應,完成反應與48小時的後處理過程後,反應的最後產率為82%。對於未優化的反應,填充至80%容量的6立方米反應器可合成35千克所需的產品,因此可以計算得VTO:
這個 VTO 值過高,在實際上代價極大,難以實現。由於其預計年需求量很大,在使用該 API 啟動 III 期試驗之前,就需要對專用工廠進行大量投資。但是優化後的反應能夠在 0.2 M 的二烯濃度下僅1小時(還需要12小時的後處理和反應器清潔時間)得到93%的產率。改進後,填充至 80% 容量的 6 立方米反應器可合成799公斤所需的產品,計算得 VTO:
經過優化後,這一合成步驟在設備和時間方面的成本顯著降低,並且更適合在標準製造設施中執行,無需對專用工廠進行巨額投資。
附加主題
[編輯]現在,製藥工藝化學家高度依賴酶促反應來生產用於合成 API 的重要手性片段。目前已篩選了可多種用於工藝藥物化學的酶。應用最廣泛的是酮還原酶和轉氨酶,但也有個別水解酶、醛縮酶、氧化酶、酯酶和脫鹵酶等的例子。[11]
現在,生物催化在工藝化學中最突出的用途之一是合成Januvia®。Januvia®是默克公司開發的一種DPP-4抑制劑,可以用於治療II 型糖尿病。傳統工藝合成路線後期需要先合成烯胺,再在銠催化下不對稱氫化得到 API 西格列汀。然而,該工藝存在諸多限制:需要在高壓氫氣環境下進行反應、過渡金屬催化劑成本高、碳處理工藝難以去除微量催化劑,並且立體選擇性不足,在最終成鹽之前需要重結晶。 [12] [13] 默克的工藝化學部門與中型生物催化公司Codexis簽約,讓Codexis為合成的最後一步開發可以大規模生產的生物催化還原胺化過程。Codexis對節桿菌進行了11輪定向進化,利用得到的細菌合成工程轉氨酶。該工程轉氨酶包含27個單獨的點突變,活性比親本酶高四個數量級。此外,該酶經過精心設計,可處理高濃度底物(100 g/L),並且對有機溶劑、試劑和轉氨基反應的副產物耐受性良好。這種生物催化路線成功地避免了化學催化加氫路線的局限性:避免了高壓反應、避免了碳處理去除過量催化劑的過程,避免了因對映選擇性不足而需要對產物進行重結晶。默克和Codexis因開發這條生物催化合成Januvia®的路線在2010年榮獲「總統綠色化學挑戰獎」。[14]
連續流製造
[編輯]近年來,用於小規模化學合成的連續流反應器的開發和優化取得了很大進展(麻省理工學院的Jamison Group (頁面存檔備份,存於互聯網檔案館)和劍橋大學的Ley Group (頁面存檔備份,存於互聯網檔案館)等在該領域處於領先地位)。對於某些反應,連續流在安全性、質量和產量方面可能具有明顯的優勢,然而這項技術在大規模合成中應用得很慢。
禮來公司的工藝化學組開發了一個純連續流過程,利用不對稱氫化得到合成LY500307需要經歷的關鍵中間體[15]。在這一關鍵合成步驟中,手性銠催化劑對映選擇性地還原了四取代烯烴。然而,要將催化劑負載量降低到商用水平,需要加以高達70個大氣壓的氫氣分壓。標準化學反應器的壓力限制約為10個大氣壓,而適用於100個大氣壓的高壓間歇式反應器則需要高額投資。對於處於化學開發初期的原料藥而言,這樣的投資顯然具有很大的風險。
另一個問題是加氫產物的共晶點不利,因此不可能通過傳統的分批合成工藝分離出超過94% ee的粗中間體。由於這一限制,製備LY500307的工藝化學路線必然涉及氫化後的動力學控制結晶步驟,以便將倒數第二個中間體的對映純度提高到>99% ee。 Eli Lilly的工藝化學團隊成功地開發了一種包括反應、後處理和動力學控制結晶模塊在內的完全連續流工藝來生產倒數第二個中間體。連續流反應器的高壓管既可用於氫化,又可用於其他高壓反應。由於不需要分批合成反應器的頂部空間,使用連續工藝反應器可以避免許多高壓反應相關隱患。此外,專為產品可擴展、連續、動力學控制結晶而設計的兩級混合懸浮混合產物去除(MSMPR)模塊可以以>99% ee進行分離,無需額外重結晶。
該連續流工藝生產144 kg關鍵中間體的產率為86%,接近分批合成工藝的90%產率。這個試驗規模的73 L流動反應器僅佔用不到 0.5 m3空間,卻實現了與理想的400 L傳統分批反應器相當的周產量。因此,與理想的分批合成工藝相比,連續流工藝在安全性、效率和產量方面均有優勢。
工藝化學學術研究機構
[編輯]利茲大學工藝研究與發展研究所 (頁面存檔備份,存於互聯網檔案館)
參考文獻
[編輯]- ^ Roughley, S. D.; Jordan, A. M. The medicinal chemist's toolbox: an analysis of reactions used in the pursuit of drug candidates. J. Med. Chem. 2011, 54 (10): 3451–79. PMID 21504168. doi:10.1021/jm200187y.
- ^ Dach, R.; Song, J. J.; Roschangar, F.; Samstag, W.; Senanayake, C. H. The eight criteria defining a good chemical manufacturing process. Org. Process Res. Dev. 2012, 16 (11): 1697–1706. doi:10.1021/op300144g.
- ^ Trost, B. M. The atom economy - a search for synthetic efficiency. Science. 1991, 254 (5037): 1471–7. Bibcode:1991Sci...254.1471T. PMID 1962206. doi:10.1126/science.1962206.
- ^ In an academic perspective, Furniss, et al., in Vogel's Textbook of Practical Organic Chemistry, describes yields around 100% as quantitative, yields above 90% as excellent, above 80% as very good, above 70% as good, above 50% as fair, and yields below this as poor.[來源請求]
- ^ Van Aken, K.; Strekowski, L.; Patiny, L. EcoScale, a semi-quantitative tool to select an organic preparation based on economical and ecological parameters. Beilstein J. Org. Chem. 2006, 2 (3): 3. PMC 1409775
 . PMID 16542013. doi:10.1186/1860-5397-2-3.
. PMID 16542013. doi:10.1186/1860-5397-2-3.
- ^ Faucher, A-M.; Bailey, M. D.; Beaulieu, P. L.; Brochu, C.; Duceppe, J-S.; Ferland, J-M.; Ghiro, E.; Gorys, V.; Halmos, T.; Kawai, S. H.; Poirier, M. Synthesis of BILN 2061, an HCV NS3 protease inhibitor with proven antiviral effect in humans. Org. Lett. 2004, 6 (17): 2901–2904. PMID 15330643. doi:10.1021/ol0489907.
- ^ Yee, N. K.; Farina, V.; Houpis, I. N.; Haddad, N.; Frutos, R. P.; Gallou, F.; Wang, X-J.; Wei, X.; Simpson, R. D.; Feng, X.; Fuchs, V. Efficient large-scale synthesis of BILN 2061, a potent HCV protease inhibitor, by a convergent approach based on ring-closing metathesis. J. Org. Chem. 2006, 71 (19): 7133–7145. PMID 16958506. doi:10.1021/jo060285j.
- ^ Zeng, X.; Wei, X.; Farina, V.; Napolitano, E.; Xu, Y.; Zhang, L.; Haddad, N.; Yee, N. K.; Grinberg, N.; Shen, S.; Senanayake, C. H. Epimerization reaction of a substituted vinylcyclopropane catalyzed by ruthenium carbenes: mechanistic analysis. J. Org. Chem. 2006, 71 (23): 8864–8875. PMID 17081017. doi:10.1021/jo061587o.
- ^ Grela, K.; Harutyunyan, S.; Michrowska, A. A highly efficient ruthenium catalyst for metathesis reactions (PDF). Angew. Chem. Int. Ed. 2002, 41 (21): 4038–4040 [2022-07-20]. PMID 12412074. doi:10.1002/1521-3773(20021104)41:21<4038::aid-anie4038>3.0.co;2-0. hdl:11370/969f537e-6d3b-425c-abfa-1b41e7d0e330
 . (原始內容存檔 (PDF)於2022-08-15).
. (原始內容存檔 (PDF)於2022-08-15).
- ^ Wei, X.; Shu, C.; Haddad, N.; Zeng, X.; Patel, N. D.; Tan, Z.; Liu, J.; Lee, H.; Shen, S.; Campbell, S.; Varsolona, R. J. A highly convergent and efficient synthesis of a macrocyclic hepatitis C virus protease inhibitor BI 201302. Org. Lett. 2013, 15 (5): 1016–1019. PMID 23406520. doi:10.1021/ol303498m.
- ^ Bornscheuer, U. T.; Huisman, G. W.; Kazlauskas, R. J.; Lutz, S.; Moore, J. C.; Robins, K. Engineering the third wave of biocatalysis. Nature. 2012, 485 (7397): 185–94. Bibcode:2012Natur.485..185B. PMID 22575958. S2CID 4379415. doi:10.1038/nature11117.
- ^ Savile, C. K.; Janey, J. M.; Mundorff, E. C.; Moore, J. C.; Tam, S.; Jarvis, W. R.; Colback, J. C.; Krebber, A.; Fleitz, F. J.; Brands, J.; Devine, P. N. Biocatalytic asymmetric synthesis of chiral amines applied to sitagliptin manufacture. Science. 2010, 329 (5989): 305–309. PMID 20558668. S2CID 21954817. doi:10.1126/science.1188934.
- ^ Desai, A. A. Sitagliptin manufacture: a compelling tale of green chemistry, process intensification, and industrial asymmetric catalysis. Angew. Chem. Int. Ed. 2011, 50 (9): 1974–1976. PMID 21284073. doi:10.1002/anie.201007051.
- ^ Busacca, C. A.; Fandrick, D. R.; Song, J. J.; Sananayake, C. H. The growing impact of catalysis in the pharmaceutical industry. Adv. Synth. Catal. 2011, 353 (11–12): 1825–1864. doi:10.1002/adsc.201100488.
- ^ Johnson, M. D.; May, S. A.; Calvin, J. R.; Remacle, J.; Stout, J. R.; Dieroad, W. D.; Zaborenko, N.; Haeberle, B. D.; Sun, W-M.; Miller, M. T.; Brannan, J. Development and scale-up of a continuous, high-pressure, asymmetric hydrogenation reaction, workup, and isolation. Org. Process Res. Dev. 2012, 16 (5): 1017–1038. doi:10.1021/op200362h.


![An illustrative example of convergent synthesis {\displaystyle {\begin{array}{|r|r|r|}\hline &{\text{Illustrative Example}}&{\text{Overall Yield}}\\\hline \color {BrickRed}{\text{Linear Synthesis}}&{\ce {A ->[85\%] B ->[85\%] C ->[85\%] Product}}&\color {BrickRed}{61.4\%}\\\hline \color {PineGreen}{\text{Convergent Synthesis}}&\left.{\begin{matrix}{\ce {A ->[85\%] B}}\\{\ce {D ->[85\%] E}}\end{matrix}}\quad \right\}{\ce {-> Product}}&\color {PineGreen}{72.3\%}\\\hline \end{array}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/6c5c7dc7065f27073d01f8a57db8d194f4baae1c)
![{\displaystyle {\text{VTO}}={\frac {{\text{nominal volume of all reactors}}[{\ce {m}}^{3}]*{\text{time per batch}}[{\ce {h}}]}{{\text{output per step}}[{\ce {kg}}]}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/c8000cea021078e77a3d9451f1684f2e176fa832)





