氧化鋅
| 氧化鋅 | |
|---|---|

| |
| |
| IUPAC名 氧化鋅 | |
| 英文名 | Zinc Oxide |
| 別名 | 鋅白 |
| 識別 | |
| CAS編號 | 1314-13-2 ? |
| PubChem | 14806 |
| EINECS | 215-222-5 |
| RTECS | ZH4810000 |
| 性質 | |
| 化學式 | ZnO |
| 摩爾質量 | 81.4084 g·mol⁻¹ |
| 外觀 | 白色固體 |
| 氣味 | 無味 |
| 密度 | 5.606g·cm-3 |
| 熔點 | 1975 °C (分解)[1] |
| 溶解性(水) | 難溶:0.0004 g/100 mL (17.8 °C) |
| 能隙 | 3.37 eV |
| 折光度n D |
2.0041 |
| 熱力學 | |
| ΔfHm⦵298K | −348.0 kJ/mol |
| S⦵298K | 43.9 J.K−1.mol−1 |
| 危險性 | |
| 歐盟危險性符號 | |
| 警示術語 | R:R50/53 |
| 安全術語 | S:S60, S61 |
| MSDS | ICSC 0208 |
| 歐盟編號 | 030-013-00-7 |
| NFPA 704 | |
| 閃點 | 1436 °C |
| 相關物質 | |
| 其他陰離子 | 硫化鋅 硒化鋅 碲化鋅 |
| 其他陽離子 | 氧化鎘 氧化汞 |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
氧化鋅是鋅的氧化物,難溶於水,可溶於酸和強鹼。它是白色固體,故又稱鋅白。它能通過燃燒鋅或焙燒閃鋅礦(硫化鋅)取得。在自然中,氧化鋅是礦物紅鋅礦的主要成分。人造氧化鋅有兩種製造方法:由純鋅氧化或烘燒鋅礦石而成。氧化鋅作為添加劑在多種材料和產品有應用,包括塑膠、陶瓷、玻璃、水泥、潤滑劑[2]、油漆、軟膏、粘合劑、填隙材料、顏料、食品( 補鋅劑)、電池、鐵氧體材料、阻燃材料[3]和醫用急救繃帶等。
氧化鋅是一種寬帶隙半導體材料,室溫下帶隙約3.3eV,激子束縛能高達60meV,有望取代GaN成為做紫外光LD和LED的材料。在光電子領域有重要應用。
化學性質
[編輯]雖然氧化鋅是白色粉末,但以紅鋅礦形式存在的氧化鋅因礦石中存在的錳和其他雜質而呈黃色或紅色[4]。氧化鋅晶體是熱色性材料,在空氣中加熱會變黃色冷卻後變回白色[5]。這種顏色的變化是在高溫環境下氧化鋅失去一小部分氧形成非整比化合物Zn1+xO所造成的,當溫度在800°C時,x等於0.00007。
氧化鋅是兩性氧化物,幾乎不溶於水,但在酸溶液比如鹽酸中會溶解:[6][7]
- ZnO + 2 HCl → ZnCl2 + H2O
鹼也能把氧化鋅固體分解成鋅酸鹽:
- ZnO + 2 NaOH + H2O → Na2[Zn(OH)4]
氧化鋅與油中的脂肪酸比如油酸、硬脂酸緩慢反應生成相應的羧酸鹽。氧化鋅和氯化鋅的水溶液混合後形成水泥狀的產物,這種水泥狀的化合物被稱為羥基氯化鋅[8],這種水泥狀材料可用於牙科材料[9]。
氧化鋅用磷酸處理後會形成水泥狀的產物磷酸鋅,磷鋅礦(Zn3(PO4)2·4H2O.)是這個反應所生成產物的主要成分之一[10],相關材料也是牙科材料[9]。
氧化鋅相當穩定,只在大約1975 °C的溫度下才發生分解生成鋅蒸汽和氧氣。將氧化鋅與碳混合後加熱後,碳能將氧化物還原為金屬單質,金屬鋅比氧化鋅更容易揮發[6]:
- ZnO + C → Zn + CO
氧化鋅與鋁粉或鎂粉劇烈反應,氧化鋅與氯化橡膠和亞麻子油的混合物受熱後會引起火災並有爆炸的危險[11][12]。
氧化鋅與硫化氫反應生成硫化鋅。這個用氧化鋅清除硫化氫的反應有商業用途(比如用於除臭劑):
- ZnO + H2S → ZnS + H2O
含有水和氧化鋅的軟膏暴露在紫外線的照射下,會生成過氧化氫[7]。
物理性質
[編輯]

晶體結構
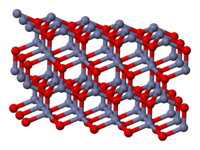
[編輯]氧化鋅晶體主要有兩種結構,六方纖鋅礦[13]和立方閃鋅礦。纖鋅礦結構最穩定因此最為常見,通過在立方晶格結構的基質上生長氧化鋅的方法來獲得立方閃鋅礦結構的氧化鋅。兩種情況下,每個鋅原子或氧原子都可以與相鄰的原子組成以其為中心的四面體結構,這是二價鋅化合物最典型的幾何結構。
除了纖鋅礦和閃鋅礦的結構,氧化鋅能在100億帕的高壓下形成氯化鈉式的八面體結構。[14]
六方的纖鋅礦和立方的閃鋅礦結構都有中心對稱性但都沒有軸對稱性[來源請求],晶體的對稱性使得纖鋅礦結構和閃鋅礦結構都有壓電效應,纖鋅礦結構的氧化鋅有焦熱電效應(Pyroelectricity)。
纖鋅礦結構的點群為6mm(赫爾曼–莫甘記號表示)或C6v(熊夫利記號表示),空間群是P63mc 。晶胞參數中,a等於3.25 Å,c等於5.2 Å,c/a比率約為1.60,接近1.633的理想六方晶胞比例[15]。在大部分由第二和第六族元素組成的半導體材料中,鋅與氧以離子鍵鍵合(Zn2+–O2–),相對應的鋅離子和氧離子半徑分別為0.074nm和0.140nm,這解釋了氧化鋅傾向於形成纖鋅礦結構而非閃鋅礦結構[16],也解釋了氧化鋅為何具有壓電效應。
氧化鋅的合成方法
[編輯]每年會生產用於工業用途的氧化鋅105噸[4],生產方法主要有三個途徑[17]。
間接法(法國)
[編輯]純的金屬鋅在石墨坩堝中熔化後,在高於907 °C(通常在1000 °C左右)的溫度下蒸發形成鋅的蒸汽,蒸汽在空氣中被氧氣氧化產生氧化鋅,這個氧化過程會發出閃亮的光同時伴隨着溫度的降低,隨後氧化鋅顆粒通過一根冷卻傳送管被收集在一個集塵室里。這個合成方法是在1844年被法國人LeClaire普及推廣開的,因此該法也被稱作法國法。此法得到的產品一般是平均尺寸0.1至幾個毫米的氧化鋅顆粒。按重量計,世界上大部分的氧化鋅是由這個方法製造的。
直接法(美國)
[編輯]直接法以不純的含鋅化合物比如爐甘石或金屬鋅精煉後的副產物為原料的,原料先用碳(比如無煙煤)加熱還原生成鋅蒸汽,接着蒸汽用間接法氧化成氧化鋅。因為原料的純度較低,所以直接法得到的最終產物相比間接法的產品質量要低一些。
化學濕法
[編輯]一小部分的工業產品是以純的鋅鹽水溶液為原料通過化學反應產生碳酸鋅或氫氧化鋅沉澱。沉澱經過過濾、洗滌、乾燥後在800°C左右的溫度下焙燒得到產品。
實驗室合成方法
[編輯]有許多專門用於合成科研和某些特定用途的氧化鋅的方法。可將這些方法根據所得氧化鋅的形態(塊狀氧化鋅、氧化鋅薄膜、氧化鋅納米線)、合成溫度(接近室溫的低溫或溫度接近1000 °C的高溫)、處理方法(氣相沉積或溶液生長)或其他參數分為多種。
大體積的單晶(體積達幾個立方厘米)通常是用氣相轉移法(氣相沉積法)、水熱合成法[18][19][20]或熔融生長法[1]製備。但是因為氧化鋅的蒸汽壓很高,所以熔融生長法不適用於培養氧化鋅單晶。氣相轉移法生長氧化鋅單晶較難控制,這使得在製備氧化鋅的單晶時傾向於使用水熱法[1]。氧化鋅薄膜的製備方法包括化學氣相沉積法、有機金屬化學氣相沉積法、電化學沉積法(Electrophoretic deposition)、脈衝激光沉積法、濺射、溶膠凝膠法、原子層沉積法、噴霧熱解法等。
實驗室中通常是用鋅棒作為陽極電解碳酸氫鈉水溶液的方法來合成氧化鋅白色粉末的。這個方法會生成氫氧化鋅和氫氣。氫氧化鋅加熱分解成氧化鋅。
- Zn + 2 H2O → Zn(OH)2 + H2
- Zn(OH)2 → ZnO + H2O
應用
[編輯]氧化鋅粉末的用途很多。大部分的用途是利用了氧化鋅的反應活性製備其他各種鋅的化合物。在材料方面,由於氧化鋅具有高折射率、優良的導熱性、抗菌和抗紫外的性質,使得它經常添加入各種材料和產品中,包括塑膠、陶瓷、玻璃、水泥、橡膠、潤滑劑[2]、油漆、軟膏、粘合劑、填隙材料、顏料、食品、電池、鐵氧體材料和阻燃材料等。[3][21]
橡膠生產
[編輯]大約50%的氧化鋅用於橡膠工業上,氧化鋅和硬脂酸連用配合可用於橡膠的硫化[17][22][23]。氧化鋅添加劑也能保護橡膠免受真菌和紫外線的破壞。
水泥工業
[編輯]水泥製造中廣泛使用氧化鋅,添加氧化鋅可以縮短處理時間、改善混凝土的防水性質[22]。
醫學上應用
[編輯]氧化鋅和0.5%氧化鐵的混合物稱為爐甘石,用於配製爐甘石洗劑。另有兩種礦物紅鋅礦和異極礦(hemimorphite)曾經也被稱為爐甘石。氧化鋅與含丁香油酚的丁香油配成的氧化鋅丁香酚(zinc oxide eugenol)可用於鑲牙和牙齒修復[9][24]。
細的氧化鋅顆粒有除臭和抗菌作用[25],所以被添加到棉織物、橡膠、食品包裝上。[26][27]細的氧化鋅顆粒比塊狀的材料抗菌作用更強,這是因為氧化鋅不是像銀那樣本身具有抗菌性[28],而是因為細的顆粒有更大的表面積。
多種用於治療各種皮膚病的日用品和藥物中都添加了氧化鋅,比如用於對付尿布皮疹的嬰兒爽身粉和護臀膏、爐甘石乳霜、有抗頭皮屑作用的洗髮精、抗菌軟膏等[29][30]。它也是一種膠布(稱為氧化鋅膠布)的主要成分,這種膠布被運動員作為繃帶使用能起到避免軟組織損傷的效果。[31]
氧化鋅能加入到乳膏、乳霜和洗液中用於保護皮膚免受紫外線引起的曬傷及其他傷害(參見防曬油)。氧化鋅能最廣泛地反射紫外光A(UVA)和紫外光B(UVB),已被美國食品藥品監督管理局批准用於防曬油中[32],而且對光穩定[33]。作為防曬油的成分之一,氧化鋅留在皮膚表面不會被皮膚吸收,起到阻擋UVA (320–400 nm)和UVB (280–320 nm)的作用。因為它和二氧化鈦一樣是起到物理防曬劑的作用而不會被皮膚吸收,所以也不會對皮膚有刺激性、不會引起過敏和痤瘡[34]。但是因為防曬劑所用的氧化鋅呈白色糊狀,粒徑超過納米尺寸會散射光線,皮膚塗抹後不夠美觀,
現在許多防曬劑使用的是氧化鋅納米顆粒配合二氧化鈦的納米顆粒,因為這些細小的顆粒不會散射光線,所以不會使皮膚顯得過分白皙。但現在還不確定納米尺寸的氧化鋅是否會被皮膚吸收[35][36]。2010年公佈的一項研究顯示氧化鋅的納米顆粒通過防曬油塗抹在人體的皮膚後被在血液和尿液中查出[37]。但來自2011年的一篇醫學研究綜述表示未在已發表的文獻中找到這些氧化鋅納米粒子會被人體系統性的吸收的證據[38]。
香煙濾嘴
[編輯]氧化鋅是香煙過濾嘴的組成部分之一用以清除煙草煙霧中的某些特定成分。濾嘴由填充了氧化鋅和氧化鐵的活性碳構成,在起到清除煙霧中的HCN和H2S作用的同時不影響煙草的味道。[21]
食品添加劑
[編輯]鋅是人體必需的營養元素,許多食品包括早餐穀物食品通過加入氧化鋅(breakfast cereals來作為鋅的來源(有時也用硫酸鋅來達到同樣的目的)。[39]一些預包裝食物即使不打算將鋅作為所含的營養素,其中也會有微量氧化鋅。
顏料
[編輯]作為油漆中的顏料[40],它比二氧化鈦的不透明性差,但比立德粉的不透明度好,氧化鋅也可用於紙張塗料。中國白(Chinese white)是特級的鋅白,可作為藝術創作所使用的顏料,也是礦物彩妝的主要成分。[41]
塗料
[編輯]含有氧化鋅的油漆早已被用於金屬的防腐蝕塗料,對鍍鋅鐵(白鐵皮)特別有效。使用有機塗料很難保護鐵質材料這是因為鐵與有機塗層的反應使得塗層變脆附着力不足,氧化鋅塗料則能保持韌性附着在鐵材料表面較長時間。[21]
參見
[編輯]參考文獻
[編輯]- ^ 1.0 1.1 1.2 Takahashi, Kiyoshi; Yoshikawa, Akihiko; Sandhu, Adarsh. Wide bandgap semiconductors: fundamental properties and modern photonic and electronic devices. Springer. 2007: 357. ISBN 3-540-47234-7.
- ^ 2.0 2.1 Hernandezbattez, A; Gonzalez, R; Viesca, J; Fernandez, J; Diazfernandez, J; MacHado, A; Chou, R; Riba, J. CuO, ZrO2 and ZnO nanoparticles as antiwear additive in oil lubricants. Wear. 2008, 265 (3–4): 422. doi:10.1016/j.wear.2007.11.013.
- ^ 3.0 3.1 Charles A. Wilkie; Alexander B. Morgan. Fire Retardancy of Polymeric Materials, Second Ed.. CRC press. 2009. ISBN 978-1-4200-8399-6.
- ^ 4.0 4.1 Klingshirn, C. ZnO: Material, Physics and Applications. ChemPhysChem. 2007, 8 (6): 782–803. PMID 17429819. doi:10.1002/cphc.200700002.
- ^ Wiberg, E. and Holleman, A. F. Inorganic Chemistry. Elsevier. 2001. ISBN 0-12-352651-5.
- ^ 6.0 6.1 Greenwood, Norman Neill; Earnshaw, Alan. Chemistry of the elements. 2016. ISBN 978-0-7506-3365-9. OCLC 1040112384 (英語).
- ^ 7.0 7.1 Spero, J. M.; Devito, B.; Theodore, L. Regulatory chemical handbook. CRC Press. 2000. ISBN 0-8247-0390-1.
- ^ Nicholson, J. W; Nicholson, J. W. The chemistry of cements formed between zinc oxide and aqueous zinc chloride. Journal of Materials Science. 1998, 33 (9): 2251. doi:10.1023/A:1004327018497.
- ^ 9.0 9.1 9.2 Ferracane, Jack L. Materials in Dentistry: Principles and Applications. Lippincott Williams & Wilkins. 2001: 70,143. ISBN 0-7817-2733-2.
- ^ Park C.-K., Silsbee M. R., Roy D. M. Setting reaction and resultant structure of zinc phosphate cement in various orthophosphoric acid cement-forming liquids. Cement and concrete research. 1998, 28 (1): 141–150. doi:10.1016/S0008-8846(97)00223-8.
- ^ International Occupational Safety and Health Information Centre (CIS) (頁面存檔備份,存於互聯網檔案館) Access date January 25, 2009.
- ^ Zinc oxide (頁面存檔備份,存於互聯網檔案館) MSDS. Access date January 25, 2009.
- ^ Fierro, J. L. G. Metal Oxides: Chemistry & Applications. 6000 Broken Sound Parkway NW, Suite 300: Taylor & Francis Group. 2006: 182. ISBN 9781420028126.
- ^ Özgür, Ü.; Alivov, Ya. I.; Liu, C.; Teke, A.; Reshchikov, M. A.; Doğan, S.; Avrutin, V.; Cho, S.-J.; Morkoç, H. A comprehensive review of ZnO materials and devices. Journal of Applied Physics. 2005, 98 (4): 041301. doi:10.1063/1.1992666.[永久失效連結]
- ^ Rossler, U. (編). Landolt-Bornstein, New Series, Group III. Vol. 17B, 22, 41B. Springer, Heidelberg. 1999.
- ^ Claus Franz Klingshirn; Bruno K. Meyer; Andreas Waag; Axel Hoffmann, Johannes M. M. Geurts. Zinc Oxide: From Fundamental Properties Towards Novel Applications. Springer. 2010-08-01: 9–10 [2011-12-09]. ISBN 978-3-642-10576-0. (原始內容存檔於2013-06-04).
- ^ 17.0 17.1 Porter, F. Zinc Handbook: Properties, Processing, and Use in Design. CRC Press. 1991. ISBN 0-8247-8340-9.
- ^ Baruah, S. and Dutta, J. Hydrothermal growth of ZnO nanostructures. Sci. Technol. Adv. Mater. (free download pdf). 2009, 10: 013001. doi:10.1088/1468-6996/10/1/013001.
- ^ Schulz, D.; et al. Inductively heated Bridgman method for the growth of zinc oxide single crystals. Journal of Crystal Growth. 2008, 310 (7–9): 1832. doi:10.1016/j.jcrysgro.2007.11.050.
- ^ Baruah, Sunandan; Thanachayanont, Chanchana; Dutta, Joydeep. Growth of ZnO nanowires on nonwoven polyethylene fibers. Science and Technology of Advanced Materials (free download pdf). 2008, 9 (2): 025009. doi:10.1088/1468-6996/9/2/025009.
- ^ 21.0 21.1 21.2 Nav Bharat Metallic Oxide Industries Pvt. Limited. Applications of ZnO. 互聯網檔案館的存檔,存檔日期2009-02-26. Access date January 25, 2009.
- ^ 22.0 22.1 Brown, H. E. Zinc Oxide Rediscovered. New York: The New Jersey Zinc Company. 1957.
- ^ Brown, H. E. Zinc Oxide Properties and Applications. New York: International Lead Zinc Research Organization. 1976.
- ^ van Noort, Richard. Introduction to Dental Materials, 2d Edition. Elsevier Health Sciences. 2002. ISBN 0-7234-3215-5.
- ^ Padmavathy, Nagarajan; Vijayaraghavan, Rajagopalan. Enhanced bioactivity of ZnO nanoparticles—an antimicrobial study. Science and Technology of Advanced Materials (free download pdf). 2008, 9 (3): 035004. doi:10.1088/1468-6996/9/3/035004.
- ^ Li, Qun; Chen, Shui-Lin; Jiang, Wan-Chao. Durability of nano ZnO antibacterial cotton fabric to sweat. Journal of Applied Polymer Science. 2007, 103: 412. doi:10.1002/app.24866.
- ^ Saito, M. Antibacterial, Deodorizing, and UV Absorbing Materials Obtained with Zinc Oxide (ZnO) Coated Fabrics. Journal of Industrial Textiles. 1993, 23 (2): 150. doi:10.1177/152808379302300205.
- ^ Akhavan, Omid; Ghaderi, Elham. Enhancement of antibacterial properties of Ag nanorods by electric field. Science and Technology of Advanced Materials (free download pdf). 2009, 10: 015003. Bibcode:2009STAdM..10a5003A. doi:10.1088/1468-6996/10/1/015003.
- ^ Harding, Fred John. Breast Cancer: Cause – Prevention – Cure. Tekline Publishing. 2007: 83. ISBN 0-9554221-0-8.
- ^ British National Formulary 2008. "Section 13.2.2 Barrier Preparations"
- ^ Hughes, G.; McLean, N. R. Zinc oxide tape: a useful dressing for the recalcitrant finger-tip and soft-tissue injury (Free full text). Arch Emerg Med. 1988, 5 (4): 223. PMC 1285538
 . PMID 3233136.
. PMID 3233136.
- ^ Sunscreen. U.S. Food and Drug Administration. [2012-08-17]. (原始內容存檔於2013-09-16).
- ^ Mitchnick, MA; Fairhurst, D; Pinnell, SR. Microfine zinc oxide (Z-cote) as a photostable UVA/UVB sunblock agent. Journal of the American Academy of Dermatology. 1999, 40 (1): 85–90. PMID 9922017. doi:10.1016/S0190-9622(99)70532-3.
- ^ What to Look for in a Sunscreen. New York Times. 2009-06-10 [2012-08-17]. (原始內容存檔於2009-06-15).
- ^ Manufactured Nanomaterials and Sunscreens: Top Reasons for Precaution (PDF). 2009-08-19 [2010-04-12]. (原始內容 (PDF)存檔於2010-07-07).
- ^ Nano-tech sunscreen presents potential health risk. ABC News. 2008-12-18 [2010-04-12]. (原始內容存檔於2010-04-13).
- ^ Gulson B; et al. Small amounts of zinc from zinc oxide particles in sunscreens applied outdoors are absorbed through human skin. Toxicol Sci. 2010, 118 (1): 140–9. PMID 20705894.
- ^ M E. Burnett and S Q Wang. Current sunscreen controversies: a critical review. Photodermatology, Photoimmunology & Photomedicine. 2011, 27: 58–67. PMID 21392107. doi:10.1111/j.1600-0781.2011.00557.x.
- ^ Quaker cereals content (頁面存檔備份,存於互聯網檔案館) Access date January 25, 2009.
- ^ Zinc Oxide as a pigment 互聯網檔案館的存檔,存檔日期2012-02-14. Access date January 25, 2009
- ^ Bouchez, Colette. The Lowdown on Mineral Makeup. WebMD. [2009-01-25]. (原始內容存檔於2009-01-23).


