磺酰氟氯
外观
| 磺酰氟氯 | |||
|---|---|---|---|
| |||
| |||
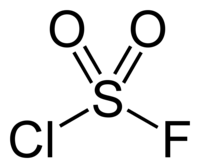
| IUPAC名 Sulfuryl chloride fluoride | |||
| 别名 | 氟氯化磺酰 | ||
| 识别 | |||
| CAS号 | 13637-84-8 | ||
| PubChem | 26159 | ||
| ChemSpider | 24370 | ||
| SMILES |
| ||
| InChI |
| ||
| InChIKey | IXPAAHZTOUOJJM-UHFFFAOYAK | ||
| ChEBI | 39445 | ||
| RTECS | WT4900000 | ||
| 性质 | |||
| 化学式 | ClFO2S | ||
| 摩尔质量 | 118.52 g/mol g·mol⁻¹ | ||
| 外观 | 无色液体或气体 | ||
| 密度 | 1.623 g/cm3(0 °C) | ||
| 熔点 | −124.7 °C(148 K) | ||
| 沸点 | 7.1 °C(280 K) | ||
| 溶解性(水) | 水解 | ||
| 溶解性(其它溶剂) | SO2、乙醚 | ||
| 结构 | |||
| 配位几何 | tetrahedral | ||
| 危险性 | |||
| 警示术语 | R:R14 R34[1] | ||
| 安全术语 | S:S24/25 S26 S27 S28 S36/37/39 S38 S45[1] | ||
| 主要危害 | 有毒,腐蚀性 | ||
| 相关物质 | |||
| 相关化学品 | SO2Cl2, SO2F2 ClSO2(NCO) | ||
| 若非注明,所有数据均出自标准状态(25 ℃,100 kPa)下。 | |||
磺酰氟氯是一种无机化合物,化学式为SO2ClF,可用作强氧化剂反应的溶剂。它可由氟代亚硫酸钾和氯气反应得到:[2]
- KSO2F + Cl2 → SO2ClF + KCl
磺酰氯和氟化钾或氟化铵在三氟乙酸中反应,也能制得磺酰氟氯:[3]
- SO2Cl2 + NH4F → SO2ClF + NH4Cl
参考文献
[编辑]- ^ 1.0 1.1 Sulfuryl chloride fluoride, distilled, 99%. [February 19, 2013]. (原始内容存档于November 17, 2015).
- ^ Seel, F.; Duncan, Leonard C.; Czerepinski, Ralph G.; Cady, George H. Sulfuryl Chloride Fluoride and Sufluryl Fluoride. Inorg. Synth. Inorganic Syntheses. 1967, 9: 111–113. ISBN 978-0-470-13240-1. doi:10.1002/9780470132401.ch28.
- ^ Prakash Reddy, V. A convenient preparation of sulfuryl chloride fluoride. Journal of Fluorine Chemistry. 1992, 56 (2): 195–197. doi:10.1016/S0022-1139(00)81102-1.


