组蛋白
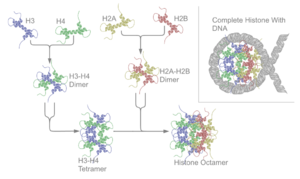
组蛋白(英语:histone,或称组蛋白)是真核生物体细胞染色质与原核细胞中的碱性蛋白质,和DNA共同组成核小体结构[1][2][3]。它们是染色质的主要蛋白质组分,作为DNA缠绕的线轴,并在基因调控中发挥作用,但是原核细胞组蛋白对基因调控的作用非常微弱[3]。没有组织蛋白,染色体中未缠绕的DNA将非常长(人类DNA中的长宽比超过1000万比1)。例如,每个人类二倍体细胞(含有23对染色体)具有约1.8米长的DNA,但是在组织蛋白上缠绕它具有大约90微米(0.09毫米)的染色质,当在有丝分裂期间复制和浓缩时,其导致约120微米的染色体[4]。
| 核心组蛋白H2A/H2B/H3/H4 | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
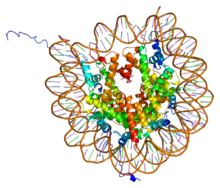 PDB rendering of Complex between nucleosome core particle (h3,h4,h2a,h2b) and 146 bp long DNA fragment based on 1aoi. | |||||||||||
| 鉴定 | |||||||||||
| 标志 | Histone | ||||||||||
| Pfam | PF00125(旧版) | ||||||||||
| Pfam宗系 | CL0012(旧版) | ||||||||||
| InterPro | IPR007125 | ||||||||||
| SCOP | 1hio / SUPFAM | ||||||||||
| |||||||||||
| 连接组蛋白H1和H5家族 | |||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|
 | |||||||||||
| 鉴定 | |||||||||||
| 标志 | Linker_histone | ||||||||||
| Pfam | PF00538(旧版) | ||||||||||
| InterPro | IPR005818 | ||||||||||
| SMART | SM00526 | ||||||||||
| SCOP | 1hst / SUPFAM | ||||||||||
| |||||||||||
分类和组蛋白变体
[编辑]存在五个主要的组织蛋白家族: H1/H5,H2A,H2B,H3和H4[2][5][6][7] 。组织蛋白H2A,H2B,H3和H4被称为核心组织蛋白(Core Histone),而组织蛋白H1/H5被称为连接组织蛋白(Linker Histone)。
在H2A、H2B、H3及H4这四种组蛋白中的其中两种称为“核心组蛋白”,并且集合成为八聚体的核小体核心颗粒。这种集合是将DNA的146对碱基对以1.65左手超螺旋形围在这个蛋白质线轴。连接组蛋白H1将核小体核心颗粒与DNA的进入位点及E位点结合,因而可以将DNA紧扣在位,并且能容许形成更高层次的结构。最基本的形状为一个10纳米的纤维或一连串的珠子。这涉及将在每一个核小体之间约50对的DNA碱基对围在这些核小体上,这些DNA又称为连接DNA。较高层次的结构包括有30及100纳米的纤维,是在一般细胞内的结构。在减数分裂中,透过核小体与其他蛋白质的相互作用,合成染色体。合成的组蛋白与DNA称为染色质。
核心组蛋白是高度保守的蛋白质,意即组蛋白在氨基酸序列中有着非常小的改变。连接组蛋白通常有着多于一种的形状,对比核心组蛋白是保守程度较低的。
在主要的组蛋白类别中,亦存在一些异构体。它们有着相同的氨基酸序列及相似的核心结构,但却有着不同的特征。这些不同的组蛋白通常带着染色质的特别功能,就如与H3相似的CenpA是唯一的组蛋白与染色体的着丝点联合;H2A的异构体H2A.Z是与活性转录基因联合与涉及在异染色体的形成;另一个H2A异构体H2A.X以双链断裂与DNA结合,并进行DNA修复。
H1
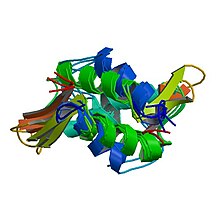
[编辑]组蛋白H1有着一个中央球状结构域及长的C与N端尾巴,能将小珠子串结构围成30纳米大小的螺线管结构。对比其他种类的组蛋白,H1的数量只为其他的一半。这是因为它不是构成核小体部分,而只是将DNA及核小体紧扣在一起。H1亦有着它的异构体,称为组蛋白H5。
H2A、H2B及H4
[编辑]组蛋白H2A、H2B及H4同样有着一个主要的球状结构域与长的N端尾巴,是组成小珠子串结构内的核小体的重要单元。
H3
[编辑]与组蛋白H2A及H2B类似,组蛋白H3有着一个主要的球状结构域与长的N端尾巴,是组成小珠子串结构内的核小体的重要原素。它的N端尾巴从球状核小体核心伸出,能进行多种影响细胞运作的表观遗传修饰。这些修饰包括将甲基及乙酰基共价附着于离氨酸或精氨酸,及丝氨酸或羟丁氨酸的磷酸化。离氨酸9的甲基化涉及基因沉默及在DNA内形成相对较不活跃的异染色质。组蛋白H3的乙酰基化会在组蛋白尾巴内不同的离氨酸位置出现,并且由组蛋白乙酰转移酶(HAT)所催化。离氨酸14的乙酰基化在基因中很普遍,亦会转录成为核糖核酸(RNA)。
以下是人类组蛋白的列表:
| 超级家族 | 家族 | 亚家族 | 成员 |
|---|---|---|---|
| 连接组织蛋白 | H1 | H1F | H1F0, H1FNT, H1FOO, H1FX |
| H1H1 | HIST1H1A, HIST1H1B, HIST1H1C, HIST1H1D, HIST1H1E, HIST1H1T | ||
| 核心组织蛋白 | H2A | H2AF | H2AFB1, H2AFB2, H2AFB3, H2AFJ, H2AFV, H2AFX, H2AFY, H2AFY2, H2AFZ |
| H2A1 | HIST1H2AA, HIST1H2AB, HIST1H2AC, HIST1H2AD, HIST1H2AE, HIST1H2AG, HIST1H2AI, HIST1H2AJ, HIST1H2AK, HIST1H2AL, HIST1H2AM | ||
| H2A2 | HIST2H2AA3, HIST2H2AC | ||
| H2B | H2BF | H2BFM, H2BFS, H2BFWT | |
| H2B1 | HIST1H2BA, HIST1H2BB, HIST1H2BC, HIST1H2BD, HIST1H2BE, HIST1H2BF, HIST1H2BG, HIST1H2BH, HIST1H2BI, HIST1H2BJ, HIST1H2BK, HIST1H2BL, HIST1H2BM, HIST1H2BN, HIST1H2BO | ||
| H2B2 | HIST2H2BE | ||
| H3 | H3A1 | HIST1H3A, HIST1H3B, HIST1H3C, HIST1H3D, HIST1H3E, HIST1H3F, HIST1H3G, HIST1H3H, HIST1H3I, HIST1H3J | |
| H3A2 | HIST2H3C | ||
| H3A3 | HIST3H3 | ||
| H4 | H41 | HIST1H4A, HIST1H4B, HIST1H4C, HIST1H4D, HIST1H4E, HIST1H4F, HIST1H4G, HIST1H4H, HIST1H4I, HIST1H4J, HIST1H4K, HIST1H4L | |
| H44 | HIST4H4 |
结构
[编辑]核小体核心颗粒是由两个H2A-H2B二聚物及两个H3-H4二聚物结合而成,形成两半接近对称的蛋白质三级结构(2阶旋转对称,即1个高分子是另一个的镜像)。H2A-H2B及H3-H4二聚物本身亦呈现伪双向对称。
这四个核心组蛋白(H2A、H2B、H3及H4)是在结构上相似及在进化中高度保存的,所有均有着一个“螺旋缠绕螺旋缠绕螺旋”的形状,可以容许简单的二聚化。它们在氨基酸结构上都有着一条长的尾巴,让转录后修饰的进行。
总括来说,组蛋白与DNA有着五种的相互作用:
- H2B、H3及H4的α螺旋两极积聚正电,能与DNA的带有负电荷的磷酸盐分子团产生相互作用。
- 在DNA骨干与氨基之间的氢键对组蛋白的主链。
- 组蛋白与DNA的脱氧核糖的非极性相互作用。
- 碱性氨基酸(如离氨酸及精氨酸)旁链与DNA磷酸氧旁链之间的盐连及氢键。
- H3及H2B的N端尾巴的非特定副槽面插入至DNA分子的两个副槽面。
组蛋白最重要的基本性质,除了是协助与DNA的相互作用外,就是它的水溶性。
组蛋白的翻译后修饰会先在它的N端尾巴开始,再而在其球状结构域进行。这种修饰包括有甲基化、瓜氨酸化、乙酰化、磷酸化、小泛素相关修饰化、泛素化及二磷酸腺苷核糖基化。这些影响着组蛋白在基因调控的功能。
一般来说,活性的基因较少与组蛋白联系,但非活性的基因会在间期中与组蛋白联合。组蛋白的结构在进化上保存,这是因为任何有害的突变会造成严重的不适应性。
历史
[编辑]于1884年,艾布瑞契·科塞尔首先发现组蛋白。直至1990年代早期,组蛋白才被更多认识,并非纯粹细胞核的惰性填充料,这部分基于马克·普塔什尼(Mark Ptashne)等人的模型,他们认为转录是被蛋白质-DNA和蛋白质-蛋白质相互作用在很大程度上被激活裸DNA模板,就像细菌一样。及后它的调控功能才被发现。
在1980年代,Yahli Lorch和罗杰·科恩伯格(Roger Kornberg)[8]表明,核心启动子上的核小体体外阻止了转录的启动,迈克尔·格伦斯坦(Michael Grunstein)[9]证明组蛋白在体内抑制转录,导致核小体为 一般基因阻遏物。
功能
[编辑]填充蛋白质
[编辑]组蛋白作为DNA缠绕的线轴。这使得能够在细胞核内将真核细胞的大型的基因组所必需的压实物:压实的分子比未压实的分子短40,000倍。
染色质调控
[编辑]组织蛋白进行翻译后修饰,以更改它与DNA及其他核蛋白的相互作用。组织蛋白H3及H4有着核小体伸出的长尾巴,能够在不同的地方进行共价修饰。这种修饰包括有甲基化、瓜氨化、乙酰基化、磷酸化、小泛素相关修饰化、泛素化及二磷酸腺苷核糖基化。组织蛋白核心(即H2A及H3)亦可以作出修饰。修饰的组合可以组成编码,成为组织蛋白编码。组织蛋白修饰在不同的生物过程起着作用,包括基因表观调控、DNA修复、有丝分裂及减数分裂 [10]。
组织蛋白修饰的命名是:
举例来说,H3K4Me就代表组织蛋白H3从N端开始起计第4个赖氨酸的甲基化。
参考文献
[编辑]- ^ Youngson RM. Collins Dictionary of Human Biology. Glasgow: HarperCollins. 2006. ISBN 0-00-722134-7.
- ^ 2.0 2.1 Cox M, Nelson DR, Lehninger AL. Lehninger Principles of Biochemistry. San Francisco: W.H. Freeman. 2005. ISBN 0-7167-4339-6.
- ^ 3.0 3.1 杨荣武, 生物化学原理第三版. 基因表达调控. 北京: 高等教育出版社. 2018. ISBN 9787040500813.
- ^ Redon C, Pilch D, Rogakou E, Sedelnikova O, Newrock K, Bonner W. Histone H2A variants H2AX and H2AZ. Current Opinion in Genetics & Development. Apr 2002, 12 (2): 162–9. PMID 11893489. doi:10.1016/S0959-437X(02)00282-4.
- ^ Histone Variants Database 2.0. National Center for Biotechnology Information. [13 January 2017]. (原始内容存档于2016-12-20).
- ^ Bhasin M, Reinherz EL, Reche PA. Recognition and classification of histones using support vector machine. Journal of Computational Biology. 2006, 13 (1): 102–12. PMID 16472024. doi:10.1089/cmb.2006.13.102.
- ^ Hartl DL, Freifelder D, Snyder LA. Basic Genetics. Boston: Jones and Bartlett Publishers. 1988. ISBN 0-86720-090-1.
- ^ Lorch Y, LaPointe JW, Kornberg RD. Nucleosomes inhibit the initiation of transcription but allow chain elongation with the displacement of histones. Cell. Apr 1987, 49 (2): 203–10. PMID 3568125. doi:10.1016/0092-8674(87)90561-7.
- ^ Kayne PS, Kim UJ, Han M, Mullen JR, Yoshizaki F, Grunstein M. Extremely conserved histone H4 N terminus is dispensable for growth but essential for repressing the silent mating loci in yeast. Cell. Oct 1988, 55 (1): 27–39. PMID 3048701. doi:10.1016/0092-8674(88)90006-2.
- ^ Ning Song, Jie Liu, Shucai An, Tomoya Nishino, Yoshitaka Hishikawa and Takehiko Koji. Immunohistochemical analysis of histone H3 modifications in germ cells during mouse spermatogenesis. Acta Histochemica et Cytochemica. 2011, 44 (4). doi:10.1267/ahc.11027.[永久失效链接]
参见
[编辑]外部链接
[编辑]- HistoneDB 2.0 - 组织蛋白和变体数据库 (页面存档备份,存于互联网档案馆) -- 在美国国家生物技术信息中心(NCBI)
- Chromatin, Histones & Cathepsin (页面存档备份,存于互联网档案馆); PMAP The Proteolysis Map-animation
