硫代硫酸鹽
外觀
| 硫代硫酸鹽 | |
|---|---|
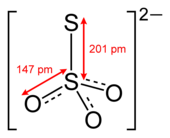
| |

| |
IUPAC名
| |
| 識別 | |
| CAS號 | 14383-50-7 |
| PubChem | 1084 |
| ChemSpider | 1054 |
| SMILES |
|
| InChI |
|
| InChIKey | DHCDFWKWKRSZHF-UHFFFAOYSA-L |
| ChEBI | 16094 |
| 性質 | |
| 化學式 | S 2O2− 3 |
| 莫耳質量 | 112.13 g·mol⁻¹ |
| 若非註明,所有數據均出自標準狀態(25 ℃,100 kPa)下。 | |
硫代硫酸鹽是含有四面體型硫代硫酸根離子(S2O32−)的一類化合物,由硫酸根離子中的一個氧被硫替換得到。最常見的硫代硫酸鹽是硫代硫酸鈉(Na2S2O3),用作照相定影劑等方面。
硫代硫酸根離子中,中心硫原子的氧化數為+5,另一個硫原子的氧化數為-1[2],平均氧化數為+2,既有氧化性也有還原性。
硫代硫酸根只在中性和鹼性環境中穩定,在酸性環境中立即分解為硫和亞硫酸根離子,進一步反應得到黃色的硫沉澱、二氧化硫氣體和水:
- S2O32−(aq) + 2H+(aq) → SO2(g) + S(s) + H2O
它也可被鹵素氧化:
- 2S2O32−(aq) + I2(aq) → S4O62−(aq) + 2I−(aq)
- S2O32−(aq) + 4Br2(aq) + 5H2O(l) → 2SO42−(aq) + 8Br−(aq) + 10H+(aq)
- S2O32−(aq) + 4Cl2(aq) + 5H2O(l) → 2SO42−(aq) + 8Cl−(aq) + 10H+(aq)
硫代硫酸根與劇毒氰化物反應生成毒性很小的硫氰酸鹽,因此硫代硫酸鈉可用作氰化物的解毒劑。常見的硫代硫酸鹽有:硫代硫酸鈉、硫代硫酸鉀、硫代硫酸銨、硫代硫酸鋇、硫代硫酸鈣、硫代硫酸金鈉等。
分析
[編輯]可溶的硫代硫酸鹽可以用二硝酸三乙二胺合鎳(II){[Ni(en)3](NO3)2}來定性分析,其反應應在中性或弱鹼性溶液中進行:
- S2O32- + [Ni(en)3]2+ → [Ni(en)3]S2O3
產生的硫代硫酸三乙二胺合鎳(II)為晶狀的紫色沉澱[3]。
參見
[編輯]參考資料
[編輯]- ^ International Union of Pure and Applied Chemistry (2005). Nomenclature of Inorganic Chemistry (IUPAC Recommendations 2005). Cambridge (UK): RSC–IUPAC. ISBN 0-85404-438-8. pp. 139,329. Electronic version.
- ^ canham, Geoff. Descriptive inorganic chemistry. City: Palgrave. 2013. ISBN 978-1-319-15411-0. OCLC 1026755795.
- ^ 無機化學叢書.第五卷.氧 硫 硒分族.北京:科學出版社,2011. 16.5.5 可溶性硫代硫酸鹽的分析. P247. ISBN 978-7-03-030544-2
