镉
镉在大多数锌矿中作为次要成分出现,并且是生产锌的副产物。镉和锌均可用作电池材料。镉可制作镍镉电池,其被用于塑胶制造和金属电镀、生产颜料、油漆、染料、印刷油墨等某些黄色的颜料、制作车胎、某些发光电子组件和核子反应堆原件。[2][3] 镉长期用作钢上的耐腐蚀镀层,镉化合物则是用作红色、橙色和黄色颜料,帮玻璃上色着色,以及稳定塑料。镉的使用正普遍减少,因为它含有毒性(它被特别列入欧洲有害物质限制[4]),且镍镉电池已被镍氢电池和锂离子电池取代。其中之一的少数新用途是碲化镉太阳能板。
虽然镉在较高等生物体中并无已知的生物功能,但在海洋硅藻中已发现了镉依赖性碳酸酐酶。
性质
[编辑]物理性质
[编辑]镉是一种柔软、有延展性、银白色的二价金属。 它在许多方面与锌相似,但会形成配合物。[5]与大多数金属不同,镉具有耐腐蚀性,可作为其他金属的保护镀层。块状的金属镉不溶于水[6]、不易燃;然而,粉末形式的镉可能会燃烧并释放有毒烟雾。[7]
化学性质
[编辑]虽然镉通常具有+2价的氧化态,它也存在+1价的状态。镉及其同族元素有时不被认为是过渡金属,因为它们在元素态或常见氧化态下不具有未填满之d或f轨域。[8]镉在空气中燃烧会形成棕色的非晶体氧化镉。该化合物的晶体呈深红色,并会随着加热而改变颜色,此性质类似于氧化锌。镉溶于盐酸、硫酸和硝酸,分别形成氯化镉、硫酸镉以及硝酸镉。若要产生氧化态+1价的镉,可将镉溶解在氯化镉和氯化铝的混合物中,会形成与Hg22+相似的Cd22+阳离子。[5]
- Cd + CdCl2 + 2 AlCl3 → Cd2(AlCl4)2
镉分别与核碱基、氨基酸及维生素分子所形成之错合物结构已被确定。[9]
同位素
[编辑]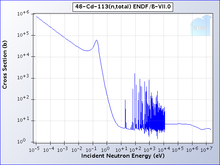
自然界中的镉由8种同位素组成。其中两种具有放射性,三种被预测会衰变不过尚未在实验室被观察到。两种自然界中具有放射性的同位素分别为113Cd(β衰变,半衰期为7.7×1015年)和116Cd(双β衰变,半衰期为2.9 × 1019年)。另外三种同位素为 106Cd、108Cd(都是双电子捕获)和 114Cd(双β衰变),对于这三种只知道半衰期的下限。至少有三种同位素——110Cd、111Cd和112Cd是稳定的。人造同位素的部分,半衰期最长的是462.6天的109Cd和53.46小时的115Cd,其余具放射性的同位素的半衰期都不到2.5小时,大多数甚至都不到5分钟。镉有8个已知的同核异构体,其中最稳定的是113mCd(t1⁄2 = 14.1 年)、115mCd(t1⁄2 = 44.6 天)和 117mCd(t1⁄2 = 3.36 小时)。[10]
镉的已知同位素的原子量范围从94.950 u(95Cd)到131.946 u(132Cd)都有。原子量小于112 u的同位素主要的衰变模式为电子捕获,而主要的衰变产物是银,但较重的同位素主要透过β衰变衰变成铟。[10]
镉-113对于吸收中子有高选择性。当中子的能量低于镉的截止能时,中子将有很大几率被吸收,而高于镉的截止能的中子将会穿透。镉的截止能大概是0.5eV,低于这个能量的中子就是慢中子。[11]
镉在一些低或中等质量的星体(0.6~10倍的太阳质量)里透过s-过程产生数千年。在此过程中,一颗银原子捕获一颗中子,然后进行β衰变。[12]
来源
[编辑]约有一千万分之一(0.1 ppm)的地壳是由镉所构成。比起构成地壳约百万分之六十五(65 ppm)的锌,镉稀少许多。目前没有已知矿物显著含镉。唯一的重要含镉矿物,硫镉矿,几乎总是和闪锌矿一起出现,因为它们在地质化学上的相似性,也几乎没有地质过程会分离它们。因此,镉通常是采矿、冶炼和提纯含硫锌矿(较小程度上,铅矿和铜矿)的副产品。少量的镉,约占总产量的十分之一,多数来自废铁和废钢的回收。美国在1907年开始生产,但在一次大战后开始大量使用。
在开采来制作磷酸盐肥料的岩石中含有不同量的镉,导致肥料中的镉浓度高达每公斤300毫克,也导致农业土壤中的高镉含量。煤炭中可能含有大量的镉,多数随着燃烧成为烟尘。土壤中的镉可以被一些农作物吸收,例如稻米。中华人民共和国农业部在2002年检测到有百分之28的稻米取样含有超过法律规范的限制的铅,而百分之10的稻米取样含有超过法律规范的限制的镉。一些植物,例如柳树和杨属植物,被发现可以清除土壤中的铅和镉污染。
生产
[编辑]根据英国地质调查局在2001年的报告,中国是镉的最大量生产者,生产了世界产量的六分之一,紧接在后的是韩国和日本。
镉是一个含锌矿物中常见的杂质,而通常会在制造锌的过程被分离。有些由含硫锌矿得到的锌矿高达百分之1.4的镉。在1970年代,出产一吨含有的锌中含有6.5磅的镉。因为氧气的存在,硫化锌矿物会被氧化成为氧化物。锌金属可以借由碳来冶炼该氧化物而产生,或借由该氧化物在硫酸中的电镀。借由真空蒸馏法,可以在冶炼锌的过程中隔离镉杂质,而硫化镉会在电解液中沉淀。
历史
[编辑]1817年,化学家卡尔·塞缪尔·莱贝雷希特·赫尔曼、弗里德里希·施特罗迈尔和罗洛夫几乎同时发现了镉元素。[13]
镉污染
[编辑]镉对健康有不良的影响,被列为可致癌物。
1930-1960年代,日本富山县神通川流域部分被镉污染,发生痛痛病,事缘炼锌厂排放的含镉废水污染了周围的耕地和水源。
广州中山大学生物科技学院联同香港浸会大学生物系在2006年3至4月期间,抽查化验中港两地市面出售的杨桃,51%镉含量属严重超标。[14]
-
可由电解氯化镉水溶液制取镉金属
-
电解法制出的镉
各地对镉安全标准
[编辑]台湾
[编辑]根据《中华民国国家标准污水综合排放标准[15]》,镉属于第一类污染物,其最高允许排放浓度为0.1mg/L。[16]
欧盟
[编辑]美国
[编辑]美国环境保护署限制排入湖、河、弃置场和农田的镉量并禁止杀虫剂中含有镉。美国环境保护署允许饮用水含有10ppb的镉,并打算把限制减到5ppb。美国食品和药物管理局规定食用色素的含镉量为不得多于15ppm。美国职业安全卫生署规定工作环境空气中镉含量在烟雾为100微克/立方米,在镉尘为200微克/ 立方米。美国职业安全卫生署计划将空气中所有镉化合物含量限制在1到5微克/ 立方米美国国家职业安全和卫生研究所希望让工人尽量少呼吸到镉以防止肺癌[18]。
参考资料
[编辑]- ^ Prohaska, Thomas; Irrgeher, Johanna; Benefield, Jacqueline; Böhlke, John K.; Chesson, Lesley A.; Coplen, Tyler B.; Ding, Tiping; Dunn, Philip J. H.; Gröning, Manfred; Holden, Norman E.; Meijer, Harro A. J. Standard atomic weights of the elements 2021 (IUPAC Technical Report). Pure and Applied Chemistry. 2022-05-04. ISSN 1365-3075. doi:10.1515/pac-2019-0603 (英语).
- ^ 存档副本. [2007-09-22]. (原始内容存档于2013-11-27).
- ^ 存档副本 (PDF). [2007-09-22]. (原始内容 (PDF)存档于2009-04-19).
- ^ Morrow, H. Cadmium and Cadmium Alloys. Kirk-Othmer Encyclopedia of Chemical Technology. John Wiley & Sons. 2010: 1–36. ISBN 978-0-471-23896-6. doi:10.1002/0471238961.0301041303011818.a01.pub3.
- ^ 5.0 5.1 Holleman, A. F.; Wiberg, E.; Wiberg, Nils. Cadmium. Lehrbuch der Anorganischen Chemie, 91–100. Walter de Gruyter. 1985: 1056–1057. ISBN 978-3-11-007511-3 (德语).
- ^ Cadmium 3.2.6 Solubility. PubChem. [25 November 2021]. (原始内容存档于2022-07-09).
- ^ Case Studies in Environmental Medicine (CSEM) Cadmium. Agency for Toxic Substances and Disease Registry. [30 May 2011]. (原始内容存档于6 June 2011).
- ^ Cotton, F. A. Survey of Transition-Metal Chemistry. Advanced Inorganic Chemistry 6th. John Wiley and Sons. 1999: 633. ISBN 978-0-471-19957-1.
- ^ Carballo, Rosa; Castiñeras, Alfonso; Domínguez-Martin, Alicia; García-Santos, Isabel; Niclós-Guttiérrez, Juan. Chapter 7. Solid state structures of cadmium complexes with relevance to biological systems. Astrid Sigel; Helmut Sigel; Roland K. O. Sigel (编). Cadmium: From Toxicology to Essentiality. Metal Ions in Life Sciences 11. Springer. 2013: 145–189. ISBN 978-94-007-5178-1. PMID 23430774. doi:10.1007/978-94-007-5179-8_7. hdl:11093/232.
- ^ 10.0 10.1 Audi, Georges; Bersillon, Olivier; Blachot, Jean; Wapstra, Aaldert Hendrik. The NUBASE evaluation of nuclear and decay properties. Nuclear Physics A. 2003, 729: 3–128. Bibcode:2003NuPhA.729....3A. ISSN 0375-9474. doi:10.1016/j.nuclphysa.2003.11.001.
- ^ Knoll, G. F. Radiation Detection and Measurement. Wiley. 2000: 505. ISBN 978-0-471-07338-3.
- ^ Padmanabhan, T. Stellar Nucleosynthesis. Theoretical Astrophysics, Volume II: Stars and Stellar Systems. Cambridge University Press. 2001: 230–236 [2022-03-30]. ISBN 978-0-521-56631-5. (原始内容存档于2022-05-21).
- ^ Cadmium. Elementymology & Elements Multidict. [2018-12-03]. (原始内容存档于2010-01-23).
- ^ 存档副本. [2007-09-22]. (原始内容存档于2014-02-28).
- ^ /, /. 中华人民共和国国家标准 污水综合排放标准 (中华民国强制性国家标准). 国家技术监督局. 1996-10-04 [2017-08-18]. (原始内容存档于2021-05-07).
- ^ GB 8978-1996 污水综合排放标准. [2012-03-09]. (原始内容存档于2021-05-07).
- ^ http://www.environment-agency.gov.uk/business/444255/446867/255244/substances/29/?any_all=&choose_order=&exactphrase=&lang=_e®ion=&searchfor=unece&subject=&theme=&withoutwords=[永久失效链接]
- ^ 存档副本. [2007-09-22]. (原始内容存档于2019-06-30).
外部链接
[编辑]- 元素镉在洛斯阿拉莫斯国家实验室的介绍(英文)
- EnvironmentalChemistry.com —— 镉(英文)
- 元素镉在The Periodic Table of Videos(诺丁汉大学)的介绍(英文)
- 元素镉在Peter van der Krogt elements site的介绍(英文)
- WebElements.com – 镉(英文)