威廉姆遜合成反應
外觀
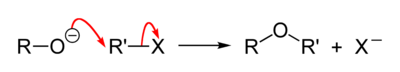
威廉姆遜合成(Williamson合成)是製備混合醚的一種方法。是由鹵代烴與醇鈉或酚鈉作用而得。是一種雙分子親核取代反應(SN2)。最早由亞歷山大·威廉·威廉姆遜發表於英國化學會志J.Chem.Soc.1852年第4卷第229頁[1]。
威廉姆遜合成法中只能選用伯鹵代烷與醇鈉為原料。因為醇鈉既是親核試劑,又是強鹼,仲、叔鹵代烷(特別是叔鹵代烷)在強鹼條件下主要發生消除反應而生成烯烴。
其反應使用的鹼取決於醇羥基的酸性,若醇是烷基醇類(羥基酸性弱)則一般都是較強的鹼,比如NaH, KH, LDA, LHMDS, NaHMDS等;而針對酚羥基這種強酸性羥基,則可以使用Na2CO3, K2CO3這樣較弱的路易斯鹼; 而有些反應甚至可以直接使用Na, K這類金屬進行氫的置換製備醇負離子。
其反應溶劑一般使用DMF,DMSO這類非質子極性溶劑,若使用乙醇一類的質子極性溶劑則非常容易讓鹵代烴發生消除反應。
其反應活性為:烷基活性:甲基> 烯丙基、苄基 > 一級碳 > 二級碳。 三級碳由於非常容易消除而很難進行取代反應。 離去基團活性: OTs、 I > OMs > Br > Cl
當反應進程中有Cu以及其鹽(比如CuI)參與時,就可以合成芳香醚類(Ullmann 反應)
醇羥基在鹼性條件下形成醇負離子,進攻鹵代烴的碳正中心,鹵代烴脫去鹵素形成醚鍵。反應條件為鹼性,高濃度鹼,高溫對反應有利;水份對反應不利[2]。
參考資料
[編輯]| 這是一篇關於化學反應的小作品。您可以透過編輯或修訂擴充其內容。 |